Physique chimie, dioxyde de
carbone .
BTS CIRA
2025.
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
.
| .. |
.
.
|
|
.
.
|
..
..
......
...
|
Fabrication du dihydrogène par vaporeformage
CH 4(g) +2H 2O(g) = CO 2(g)
+ 4H 2(g).
A - Mesure et conditionnement de la température d'entrée du gaz naturel.
On utilise une sonde de température "Pt100".
1. Que signifie
les termes "Pt" et "100" ?
Pt : matériau constituant le capteur, le platine.
100 : valeur ohmique de la résistance du capteur à 0°C.
R T = R 0(1+ aT).
T : température en degré Celcius.
2. Montrer que R 0
= 100 ohms et a =
3,8 10 -3 °C -1.
Si T = 0°C, R T = R 0 = 100 ohms.
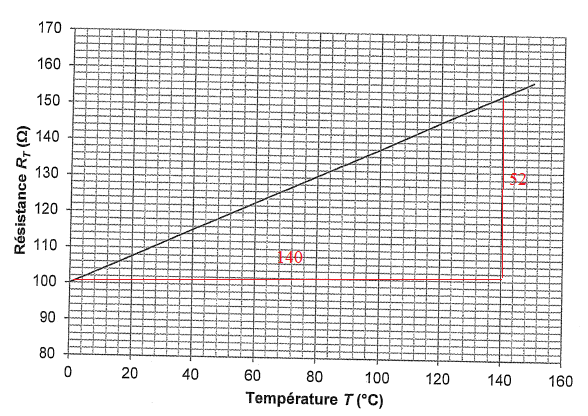
Coefficient directeur de la droite R 0a = 52 / 140 =0,38.
a =
0,38 / 100 = 3,8 10-3
°C-1.
3. Indiquer les
valeurs de la résistance R80 et R120.
R80 = 100 (1+3,8 10-3 x80)=130 ohms ( valeur lue
sur le graphique).
R120 = 100 (1+3,8 10-3 x120)=146
ohms ( valeur lue sur le graphique).
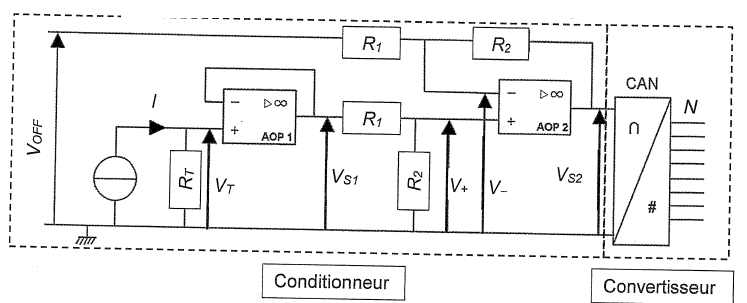
Q4. Expliquer
pourquoi les AOP1 et AOP2 idéaux fonctionnent en régime linéaure.
La tension entre les deux entrées est nulle.
Q5. Exprimer VT
en fonction de I, R0, a et T.
VT = RT I = R0(1+aT)
I.
Q6. I = 10 mA.
Déterminer les valeurs prises par VT pour T = 80 °C et 120°C.
V80 = 0,010 x130 = 1,3 V.
V120 = 0,010 x146 = 1,46 V.
Q7. Préciser les
fonctions remplies par l'AOP1.
Montage suiveur : VT = VS1.
Q8. En déduire les
valeurs prises par VS1 pour T = 80°C et 120°C.
1,3 et 1,46 V.
La tension de sortie de l'AOP2 s'exprime par : VS2 = R2
/ R1 (VS1-Voff). ( montage
soustracteur amplificateur).
Q9. Calculer Voff
et le rapport R2/R1 dans les conditions suivantes
:
T =80 °C et VS2 = 0,000 V.
0 = R2 / R1
(1,3-Voff).
Voff = 1,3 V.
T
=120 °C et VS2 = 5,00 V.
5,0 = R2 / R1
(1,3-Voff).
Partie B. Conversion analogique-numérique.
Un CAN 8 bits est placé en sortie du conditionneur. Il convertit les
tensions comprises entre 0 et 5,000 V.
10. Calculer la
valeur du quantum q du convertisseur.
q= Vréf / (28-1) =5 /(28-1)= 0,0196 V
= 19,6 mV.
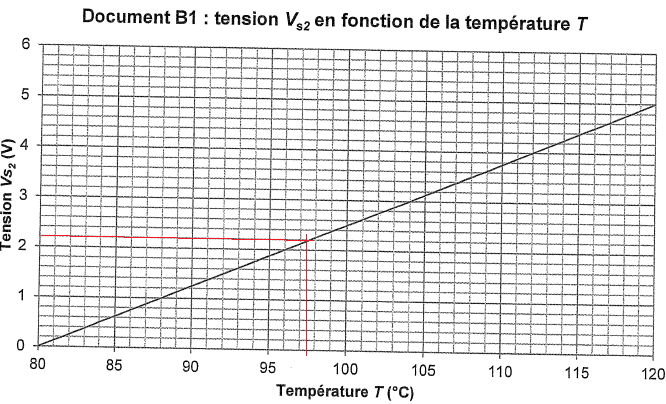
Le gaz naturel doit être chauffé jusqu'à stabilisation de la
température dans l'intervalle de tolérance [95 °C ; 105 °C].
Le procédé étant en fonctionnement, le CAN indique une valeur en
base 10 : Nbase 10 = 113.
11. Déterminer si
la température T du gaz mesurée par la sonde est compatible avec la
tolérance de température.
Usortie = q Nbase 10=0,0196 x113=2,215 V.
Par lecture graphique T =97,5°C, valeur appartenant
à [95 °C ; 105 °C].
|
...
= =
|
....
|
C
- Vaporeformage
Première étape : CH4(g) +H2O(g)
= CO(g) +3H2(g).
12. Calculer la
variation d'enthalpie DfH°
de cette réaction à 25°C.
DfH°
=DfH°
(CO) + 3 DfH°
(H2) -DfH°(H2O)
-DfH°
(CH4)= -110 +242 +75=207 kJ / mol.
13. Indiquer si la
réaction est endothermique, exothermique ou athermique.
DfH°
>0, réaction endothermique.
14. Justifier
l'intérêt d'imposer une température très supérieure à 25°C.
Une réaction endothermique est favorisée par une hausse de température.
l'équilibre est alors déplacé dans le sens direct.
15. Donner le rôle
d'un catalyseur et indiquer le type de catalyse mis en jeu.
Un catalyseur rend plus rapide une réaction thermodynamiquement
possible. La catalyse est hétérogène ( réactifs gazeux et
catalyseur solide).
Seconde étape : CO(g) + H2O(g) = CO2(g) +H2(g).
La vapeur d'eau est en excès.
16 Justifier
l'intérêt de cet excès.
Le réactif vapeur d'eau étant en excès, l'équilibre est déplacé dans le
sens direct, formation de dihydrogène.
D. Dimensionnement de
l'échangeur.
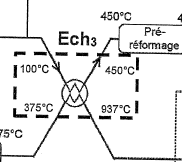
17. Indiquer le
type de circulation et préciser les températures d'entrée et de sortie
du fluide chaud puis celles du fluide froid.
Contre courant.
Fluide froid noté 2: entrée à tE=100°C, sortie à tS=
450°C.
Fluide chaud noté 1: entrée à TE=937°C, sortie à TS=375°C.
Les vapeurs venant du four entre dans l'échangeur avec un débit en
masse Qm = 2,0 kg /s. Elles possèdent une capacité
thermique massique Cp = 11,0 kJ K-1 kg-1.
18. Déterminer la
surface de l'échangeur.
Coefficient de l'échangeur K = 40 W K-1 m-2.
Puissance thermique échangée par un fluide : P = Qm Cp
DT.
Puissance thermique échangée entre deux fluides dans
l'échanheur : P =K S DTm.
DTm
=[(TE-tS)-(TS-tE)
] / ln [(TE-tS) /(TS-tE) ].
TE : température d'entrée du fluide 1 ; TS :
température de sortie du fluide 1 ;
tE : température d'entrée du fluide 2 ; tS :
température de sortie du fluide 2.
P = Qm Cp DT=2
x 11 x(937-375)=12 364 kW.
DTm
=[(TE-tS)-(TS-tE)
] / ln [(TE-tS) /(TS-tE) ]
= [(937-450) -(375-100)] / ln[(937-450) / (375-100)]=212 / 0,57=371.
P=12 364 =40 x 371 S.
S =12 364 / (40 x371)=0,83 m2.
E. Modification du débit
dans un échangeur.
La circulation des fumées est assurée par un moteur hexapolaire
alimenté par un réseau triphasé 400 / 690 V de fréquence 50 Hz.
Le schéma de la plaque à bornes de ce moteur est donné :
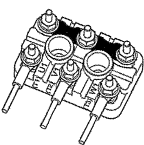
19. Identifier le
type de couplage et expliquer s'il permet au moteur de
fonctionner correctement.
Montage étoile ; tension aux bornes de chaque bobine 400 V.
Fonctionnement correct.
20. Le glissement
du moteur est g = 2 %. déterminer la vitesse de rotation du moteur en
tours par minute.
Vitesse de rotation = fréquence / nombre de paires de pôles = 50
/3 tours / seconde.
50 / 3 x 60 = 200 tr / min.
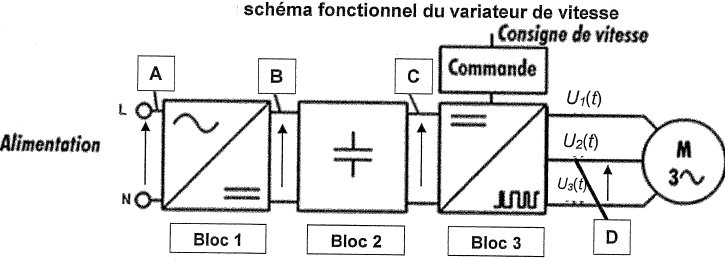
21. Donner le nom
des trois blocs intervenant dans ce variateur de vitesse.
Redresseur ; circuit intermédiaire agissant sur le
"lissage" de la tension de sortie du redresseur ; électronique de
commande.
22. Associer
chacune des tensions proposées aux points A, B, C et D du schéma.
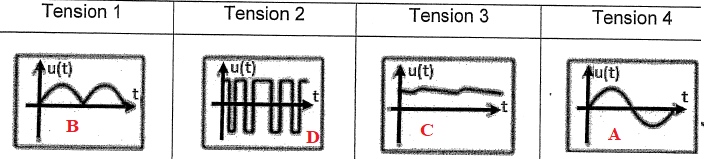
23. Expliquer
pourquoi le variateur de vitesse permet de contrôler le débit de fluide
chaud dans l'échangeur Ech1.
Le variateur de vitesse adapte la vitesse de rotation du moteur et en
conséquence le débit du fluide.
F. Stockage du dioxyde de
carbone.
Une fois isolé et purifié, le dioxyde de carbone est transporté via un
pipeline terrestre. Afin d'assurer son transport et son stockage, ce
gaz est comprimé à 80 bar et porté à 40°C.
24. Expliquer
pourquoi il est important de contrôler l'émission de dioxyde de carbone
dans l'atmosphère.
Le dioxyde de carbone est un gaz à effet de serre, contribuant au
réchauffement de l'atmosphère.
25. Compléter avec
les termes suivants : solide, liquide, vapeur, supercritique.

26. Donner les
noms attribués aux points A et B.
A : point triple ; B : point critique.
27. Indiquer
l'état dans lequel se trouve le dioxyde de carbone lorsqu'il est
transporté et stocké. Positionner cet état à l'aide d'un point E.
P = 40 bars ; T = 273+40 = 313 K. Etat liquide.
28. Tracer le
diagramme de prédominance des espèces CO2,H2O, HCO3-
et CO32-.
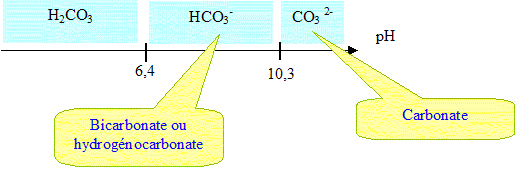
La mesure du pH de l'eau de
rivière à proximité d'un puits d'injection est 7,8.
29. Quelle espèce
prédomine dans cette eau.
HCO3-
prédomine.
On procède à un prélèvement de 100,0 mL de cette eau. La prise d'essai
est titrée par de l'acide chlorhydrique de concentration Ca = 0,020 mol
/ L.
30. Déterminer la
valeur du TAC de cett eau.
Valeur du volume ( mL) d'acide fort à 0,020 mol /L nécessaire pour
doser 100 mL de cette eau en présence de vert de bromocrésol.
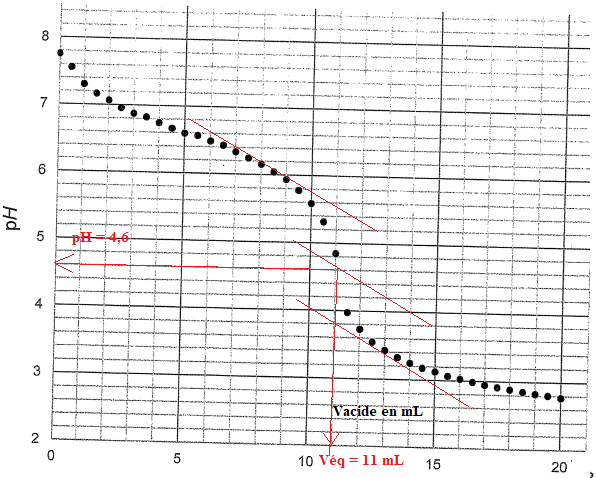
TAC = 11.
31. Préciser si le
stockage de CO2 a eu un impact sur le TAC de cette eau.
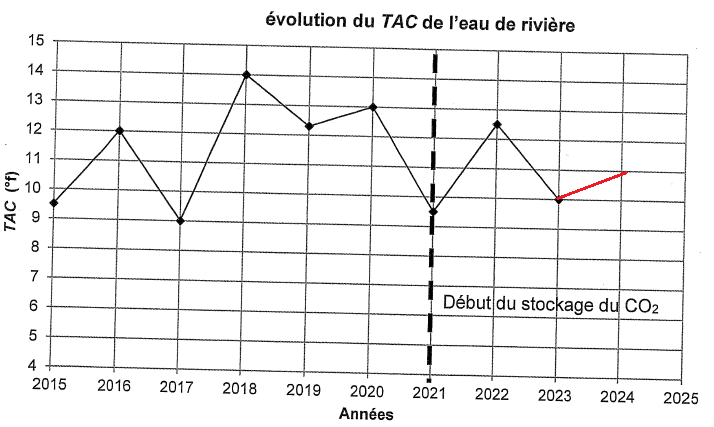
Pas d'impact en 2024 sur le TAC de cette eau.
|
|
|
|