Four
à micro-ondes pour synthèse organique.
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
..
..
|
|
Les trois étapes de la synthèse de la phényltoïne sont représentées :
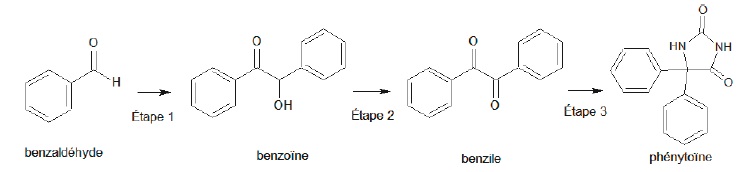
1. Préparation de la benzoïne.
On utilise un four à micro-ondes pour cette synthèse catalysée par le chlorure de thiamine.
a-
dans un erlenmeyer de 100 mL, introduire 1,35 g de chlorure de
thiamine, environ 4 mL d'eau, 15 mL d'éthanol à 95 %, 7,0 mL d'une
solution aqueuse d'hydroxyde de potassium de concentration 1,1 mol /L
puis agiter à température ambiante.
b- ajouter 20 mL de benzaldehyde.
c- recouvrir d'un
entonnoir et chauffer à l'aide du micro-ondes pendant une minute à la
puissance de 600 W, sortir du four et laisser cristalliser à
température ambiante puis refroidir dans un bain eau-glace.
d- filtrer sur
Büchner, laver les cristaux avec de l'eau glacée et les rincer avec un
mélange refroidi eau-érthanol ; on obtient des cristaux blancs.
e- purifier le produit à l'aide d'une recristallisation dans l'éthanol.
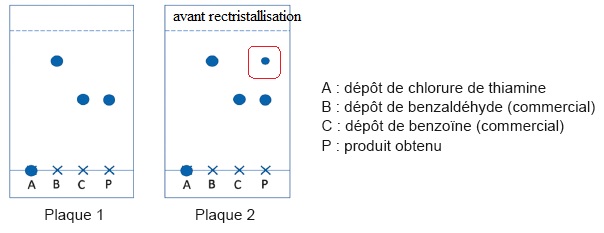
On réalise deux chromatographies CCM des cristaux obtenus ; une avant l'étape de recristallisation et une après cette étape.
1.1-
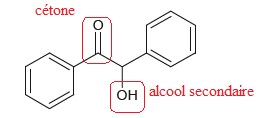
Recopier la formule topologique de la benzoïne. Entourer les groupes
caractéristiques et nommer les familes fonctionnelles correspondantes.
1.2.
Déterminer la valeur de la masse d'hydroxyde de potassium solide à
prélever pour préparer les 100,0 mL de solution aqueuse
d'hydroxyde de potassium utilisée dans l'étape a.
7,0 x1,1 =7,7 mmol. M(KOH) =56,1 g / mol.
m = 56,1 x7,7 = 431,97 mg ~0,43 g.
1.3- Donner l'état physique du produit obtenu à la fin de l'étape c.
Cristaux solides.
1.4- Indiquer la plaque qui correspond à la CCM effectuée avant la purification. Justifier.
La plaque n°2 : le produit P contient encore des traces de benzaldehyde, contrairement à la plaque n° 1.
1.5. Proposer une autre méthode d'identification du produit obtenu en fin de cristallisation.
Mesure de la température de fusion, spectroscopie IR ou RMN du proton.
Préparation du benzile.
Oxydation de la benzoïne.
2.1. Donner la formule brute de la benzoïne.
C14H12O2.
2.2.
Justifier , à partir de la demi-équation électronique associée au
couple benzile / benzoïne, que cette étape correspond bien à une
oxydation de la benzoïne.
En milieu acide : C14H12O2 --> C14H10O2 +2H+ +2e-.
En milieu basique : C14H12O2 +2HO- --> C14H10O2 +2H2O +2e-.
La benzoïne cède deux électrons : c'est un réducteur qui s'oxyde.
|
Préparation de la phénythoïne.
On
utilise un micro-ondes, en milieu basique, en utilisant l'éthanol comme
solvant. On introduit 1,00 g de benzile et 0,450 g d'urée. Après
réaction on obtient 1,11 g de phénythoïne.
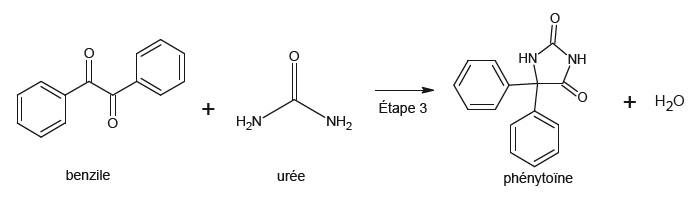
Calculer le rendement de cette étape.
Quantité de matière des réactifs :
urée : M =60,1 g / mol ; n1 =0,450 / 60,1 =7,49 10-3 mol = 7,49 mmol ( en excès ) ;
benzile : M =210,2 g / mol ; n2 = 1,00 / 210,2 =4,76 10-3 mol = 4,76 mmol.( en défaut).
Quantité de matière théorique de phénylthoïne : 4,76 mmol.
M(phénylthoïne) =252,3 g / mol.
masse théorique de phénylthoïne : 252,3 x 4,76 10-3 =1,20 g.
Rendement = masse réelle / masse théorique = 1,11 / 1,20 ~0,925 ( 92,5 %).
|
|



