|
bac
S Polynťsie
2007 : du jus de
citron dans la confiture
; titrage acide
ascorbique. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Une confiture doit Ítre prise ; les fruits, cuits avec du sucre et parfois du citron, formant une p‚te suffisamment ťpaisse. c'est la pectine des fruits, longue chaÓne molťculaire de la famille des glucides, qui est la principale responsable de cette prise. Lors de la cuisson de la confiture, les fruits se disloquent, libťrant la pectine qui passe dans le jus sucrť. En refroidissant, les molťcules de pectine forment un rťseau en s'accrochant les unes aux autres par des liaisons appelťes liaisons hydrogŤne. Celles-ci se font entre les fonctions dites acides et alcooliques qui jalonnent la molťcule de pectine, fonctions qui doivent rester libres et intactes pour ne pas entraver la formation de ce rťseau. Or l'eau qui se lie facilement ŗ ces fonctions, risque de prendre la place. Ainsi du sucre qui capte l'eau en excŤs est ajoutť. De plus, du jus de citron ťvite que les fonctions acides de la pectine ne se dissocient. Extrait du site : http://www.espace-sciences.org Document 2 : Ajoutť ŗ 1 kg de fruits, le jus d'un petit citron suffira ŗ donner l'aciditť nťcessaire pour que la pectine rťagisse (...) Le jus de citron permet en outre d'ťviter l'oxydation des fruits quand on les coupe et de leur conserver une belle couleur, notamment les fruits jaunes qui changent trŤs facilement de teinte. Extrait de : Larousse des confitures, Ed. Larousse. Donnťes : La pectine est une longue molťcule comportant des groupements acide -COOH et alcool. On la notera simplement en ne mettant en ťvidence qu'un groupe acide RCOOH. Le jus de citron contient entre autres acides, de l'acide citrique ( ŗ la concentration d'environ 0,40 mol/L) et de l'acide ascorbique ŗ une concentration moindre. L'acide ascorbique ou vitamine C( C6H8O6) peut donner lieu ŗ la demi-ťquation ťlectronique suivante : C6H8O6 = C6H6O6+ 2H+ + 2e-. Formation du gel :
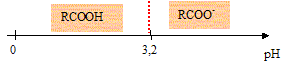
- Le pKa du couple RCOOH / RCOO- est ťgal ŗ 3,2. Placer sans justifier sur un axe de pH les domaines de prťdominance des formes acide et basique de la pectine. - Utiliser le diagramme prťcťdent pour commenter la phrase " le jus d'un petit citron suffira ŗ donner l'aciditť nťcessaire pour que la pectine rťagisse".
Equation de la rťaction de la pectine RCOOH avec l'eau : RCOOH (aq) + H2O= RCOO-(aq) + H3O+(aq). Domaines de prťdominance des formes acide et
basique de la pectine.
" le jus d'un petit citron suffira ŗ donner l'aciditť nťcessaire pour que la pectine rťagisse" La pectine peut rťagir si elle se trouve sous forme acide, c'est ŗ dire si le pH est infťrieur ŗ pKa : le groupe -COOH est alors disponible ( non dissociť ). Le jus acide du citron permet d'obtenir un pH infťrieur ŗ 3,2.
Conservation des fruits : A partir des documents proposťs pourquoi peut-on dire que l'acide ascorbique est un anti-oxydant ? Quel autre mot peut-on utiliser plutŰt que
"anti-oxydant" ŗ propos de l'acide ascorbique ?
Justifier.
Un petit citron permet d'obtenir 6,2 mL de jus filtrť. Ce jus est introduit dans une fiole jaugťe de 100,0 mL que l'on complŤte avec de l'eau dťminťralisťe. On obtient 100,0 mL de solution S. On prťlŤve alors un volume v1= 20,0 mL de solution S que l'on introduit dans un erlenmeyer. On ajoute un volume v2 = 20,0 mL de solution de diiode de concentration c2 = 2,00 10-3 mol/L. La couleur initialement brune du milieu rťactionnel s'ťclaircit peu ŗ peu, mais ne disparaÓt pas. L'ťquation de la rťaction totale qui se produit est : C6H8O6 + I2 = C6H6O6+ 2H+ +2I-. (1)
Pourquoi peut-on dire que l'acide ascorbique est un anti-oxydant ? "Le jus de citron permet en outre d'ťviter l'oxydation des fruits " L'acide ascorbique ou vitamine C( C6H8O6) peut jouer le rŰle de rťducteur et s'oxyder ŗ la place des fruits suivant : C6H8O6 = C6H6O6+ 2H+ + 2e-. ( oxydation d'un rťducteur : des ťlectrons sont libťrťs )
" La couleur initialement brune du milieu rťactionnel s'ťclaircit peu ŗ peu, mais ne disparaÓt pas" L'observation de l'ťvolution de la couleur du mťlange du milieu rťactionnel indique que : - le diiode est en excŤs : la solution finale n'est pas incolore et le diiode est la seule espŤce colorťe. - la transformation est lente : en consťquence elle ne peut pas servir de support d'un titrage. Quantitť de matiŤre n de diiode ayant rťagi avec les ions thiosulfate :
n-xE=0 donne n= -xE ; n= Ĺc3v3. n= 0,5 * 5,00 10-3 *14,5 10-3 ; n = 3,6 310-5 mol. Concentration de l'acide ascorbique dans le jus de citron testť :
v1 c1 -xf donne v1 c1= xf ; v1 c1=v2 c2 - n ; c1=(v2 c2 - n) / v1. c1 = (2,00 10-3 * 20,0 10-3 - 3,63 10-5) / 20,0 10-3 = 1,85 10-4 mol/L. Soit 1,85 10-5 mol dans la fiole jaugťe de 0,1 L, ou dans 6,2 mL de jus de citron. D'oý : 1,85 10-5 / 6,2 10-3 =3,0 10-3 mol/L. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|