|
Ammoniac : structure, propriťtťs basiques, complexes, pile Mines 2002. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| .
. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
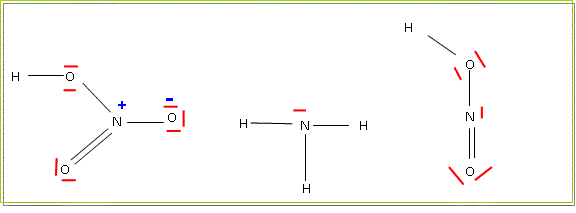
Prťciser la structure ťlectronique de l'azote (Z=7). 1s2 2s2 2p3. Ecrire les structures de Lewis de NH3, HNO2, HNO3 (l'azote est au centre) Prťciser les charges formelles portťes par les atomes.
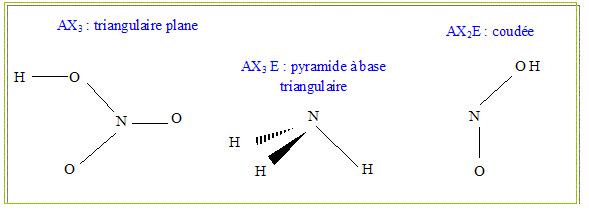
En utilisant la thťorie de la V.S.E.P.R, indiquer la gťomťtrie de NH3, HNO2, HNO3 .
Pourquoi l'analogue
n'existe-t-il pas dans la chimie de
l'azote ? L'atome de phosphore est plus volumineux que
l'atome d'azote et il possŤde de plus, une
couche 3d de valence : les propriŤtťs
du phosphore sont donc assez diffťrentes de
celle de l'azote.
Les propriťtťs complexantes de NH3 avec l'ion cuivre II. On dťfinit les constantes de formation globale de complexation, bn, les constantes de loi d'action de masse pour les rťactions : Cu2+ + nNH3 = Cu(NH3)n2+. Ecrire les expressions
de bn
Ecrire les expressions des constantes de dissociations successives Kdj : Cu(NH3)j2+
=Cu(NH3)j-12+ +
NH3.
[Cu(NH3)22+][NH3]
[Cu(NH3)32+][NH3]
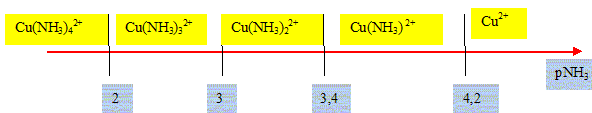
En dťduire les valeurs numťriques de dKdj = -logKdj. = 4,2 7,6-4,2 = 3,4 = 10,6-7,6 = 3 12,6-10,6 = 2
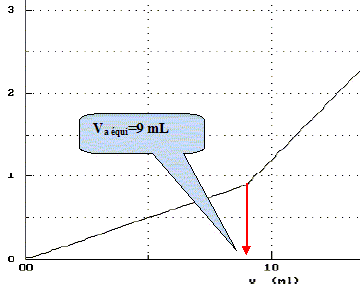
On considŤre un bťcher de 50 mL contenant un mťlange de 20 mL d'une solution d'ammoniaque 1 mol/L et de 20 mL d'une solution de sulfate de cuivre (II), CuSO4 , de concentration C1 = 0,01 mol.L-1. Expliquez pourquoi Cu(NH3)42+ est majoritaire. Ecrire la rťaction globale. [NH3]=20*1/(20+20) = 0,5 mol/L d'oý pNH3= -log 0,5 = 0,3, valeur infťrieure ŗ2. D'aprŤs le diagramme de rťpartition ci-dessus, Cu(NH3)42+ est majoritaire. Cu2+ + 4NH3 = Cu(NH3)42+. Quelles sont les concentrations de NH3, Cu2+ , Cu(NH3)42+ ŗ l'ťquilibre.
L'ammoniac ťtant en large excŤs :xťq ~0,2 mmol ; [NH3] ~ (20-4*0,2) / 40 ~0,48 mol/L ; [Cu(NH3)42+]~ 0,2/40 ~5 10-3 mol/L.
On constitue la pile suivante ŗ 25įC : - le compartiment A comporte une ťlectrode de cuivre plongeant dans une solution de sulfate de cuivre II, CuSO4 , de concentration C1 = 0,01 mol.L-1 dans un bťcher de 50 mL. - Le compartiment B comporte une ťlectrode de cuivre plongeant dans un bťcher de 50 mL contenant un mťlange de 20 mL d'une solution d'ammoniaque de concentration C2 = 1 mol/L et de 20 mL d'une solution de sulfate de cuivre II, CuSO4 , de concentration C2 = 0,01 mol.L-1. Ecrire l'expression du potentiel de Nernst pour le couple Cu2+/Cu. En dťduire la diffťrence de potentiel UAB . E1 = Eį(Cu2+/Cu) + 0,03 log [Cu2+]1 ; E2 = Eį(Cu2+/Cu) + 0,03 log [Cu2+]2 ; UAB = E1-E2 = 0,03 log [Cu2+]1 /[Cu2+]2 =0,03 log (0,01 / 2,4 10-14) = 0,35 V. Faire le schťma de la pile. Prťciser la borne (+) et (-). + Cu | Cu2+|| Cu(NH3)42+ | Cu - Ecrire les rťactions ŗ l'anode et ŗ la cathode. Oxydation du cuivre de l'ťlectrode ŗ l'anode nťgative : Cu + 4 NH3 = Cu(NH3)42+ + 2e-. Rťduction ŗ la cathode positive de Cu2+ : Cu2+ + 2e- = Cu . Donner le bilan de la rťaction dans le cas oý on laisserait la pile dťbiter. Cu2+ +4 NH3 = Cu(NH3)42+. Quel est le rŰle du pont salin ? Assure la continuitť ťlectrique et l'ťlectroneutralitť des solutions.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||