|
Pondichéry 04/ 02 En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts. |
|||||||||||
|
|||||||||||
|
|
Données : L'eau de Javel est un produit courant utilisé pour son pouvoir désinfectant. Elle peut être obtenue en dissolvant du dichlore gazeux dans une solution aqeuse d'hydroxyde de sodium selon l'équation bilan / (1) Cl2 + 2Na+ + 2HO- --> ClO- + Cl- + 2Na+ + H2O Lors de la préparation de l'eau de Javel, les ions hydroxydes sont introduits en excès. Le pH de l'eau de Javel est compris entre 11 et 12. Les propriétés de l'eau de Javel sont dues au caractère oxydant des ions hypochlorites ClO-. Ces ions peuvent donner lieu à divers réactions, dans lesquelles interviennet divers facteurs : pH, concentrations, température, catalyseurs (ions métalliques), rayonnements (UV). En particulier, les ions hypochlorites réagissent en présence d'eau : - en milieu basique : (2) ClO---> Cl- + ½ O2. - en milieu acide : (3) ClO- + Cl- + 2H3O+ --> Cl2 + 3H2O Quelques recommandations lues sur les emballages d'eau de Javel : - Conserver au frais, à l'abri du soleil et de la lumière. - Ne pas utiliser en combinaison avec d'autres produits : au contact d'un acide, dégage un gaz toxique Concentration d'une eau de Javel : Elle est souvent définie par le degré chloromètrique(°chl). Il correspond au volume ( exprimé en litres) de dichlore gazeux, mesuré dans les conditions normales de température et de pression, qu'il faudrait utiliser pour fabriquer 1 L de cette eau de javel selon l'équation bilan (1). dans ces conditions le volume molaire est Vm =22,4 L/mol.
Les réponses qualitatives doivent être justifiées.
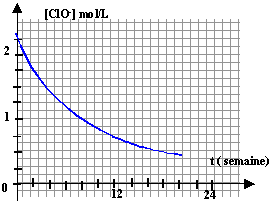
d'après les coefficients de l'équation (1) : 2,143 mol ion hypochlorite ClO- dans 1 L de solution [ClO-]
= 2,143 mol/L.
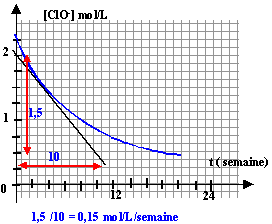
cette vitesse est représentée par la valeur absolue du coefficient directeur de la tangente à la courbe à la date considérée:
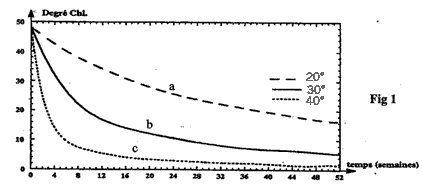
la température : à une date donnée, la valeur absolue du coefficient directeur de la tangente à la courbe augmente de la courbe a ( 20°C) à la courbe c ( 40°C) : la vitesse de disparition de ClO- augmente avec la température. la concentration des réactifs : pour une courbe donnée ( pour une température donnée) , la valeur absolue du coefficient directeur de la tangente à la courbe diminue au cours du temps ( tangente moins inclinée sur l'horizontale). La vitesse de disparition de ClO- diminue si la concentration des réactifs diminuent. En conservant au frais, la vitesse de disparition du principe actif, l'ion hypochlorite est plus faible : l'eau de Javel conserve un plus longtemps ces propriétés. Les berlingots
sont plus concentrés ( 4 fois plus) en ion hypochlorite que les flacons
: en conséquence la vitesse de disparition de l'ion hypochlorite est 4
fois plus grande dans un berlingot que dans un flacon ; d'où
l'indication d'un date limite écrite sur le berlingot.
En présence de lumière solaire ( UV) la diparition de l'ion hypochlorite est accélérée : d'où la conservation de l'eau de Javel dans un flacon opaque.
|
||||||||||
| |
|||||||||||
|