|
|
||||||
|
fer et aluminium |
On place dans une eau désaérée un fil d'aluminium. Il ne se produit rien. Le même fil placé dans une solution d'acide chlorhydrique à 0,1 mol L-1 conduit à un dégagement faible de dihydrogène. Si on met en contact avec le fil un clou en fer, le dégagement est intense. Expliquer ces phénomènes. 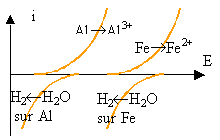
corrigé |
|||||
|
|
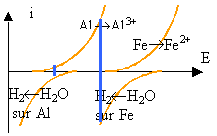
Dans l'eau pure il ne se passe rien, car l'aluminium est recouvert d'un film d'alumine protecteur. Dans la solution d'acide chlorhydrique, une fois ce film détruit l'attaque du métal débute. Les courbes intensité potentiel indiquent une intensité du courant assez faible : le dégagement est donc faible. En présence d'un clou en fer, l'aluminium est attaqué, étant plus réducteur que le fer et les courbes indiquent une intensité importante : le dégagement de H2 est important.
|
|||||
|
accumulateur au plomb |
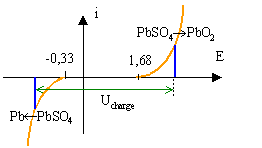
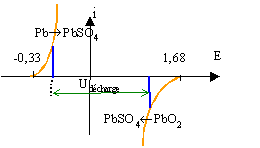
Cet accumulateur est constitué de 2 plaques plongeant dans l'acide sulfurique. Les couples suivants interviennent : PbO2 / Pb et PbSO4 / Pb.
E (PbO2 / Pb)=1,68 V ; E(PbSO4 / Pb) =-0,33 V. corrigé |
|||||
|
|
PbSO4 + 2H2O --> PbO2 +2e- + 4H+ +SO42-oxydation de PbSO4. PbSO4 + 2 e--->Pb + SO42- réduction de PbSO4.
décharge Pb + SO42- --> PbSO4 + 2 e-. oxydation du plomb PbO2 +2e- + 4H+ +SO42- --> PbSO4 + 2H2O réduction de PbO2.
U décharge est inférieure à U charge : on fournit plus d'énergie que l'on en récupère.
|
|||||
|
|
|