L'atropine.
Bac
Amérique du Nord
2025.
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
.
| . |
.
.
|
|
.
.
|
..
..
......
...
|
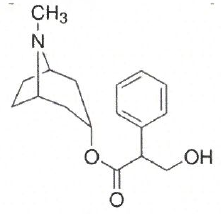
Etude des ampoules pharmacologique d'atropine.
Q1. Construire le diagramme de prédominance du couple acide /base de l'atropine.
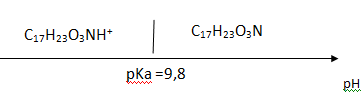
Concentration en masse d'atropine dans une ampoule :Cma =25 mg / L.
Volume d'une ampoule Va =20 mL ; pH ~ 4.
Q2. Sous quelle forme se trouve l'atropine dans l'ampoule.
A pH < pKa, la forme C17H23O3NH+ prédomine.
Q.3. Calculer la concentration des ions oxonium de la solution dans l'ampoule.
[H3O+] = 10-pH = 1,0 10-4 mol / L.
Q.4. Calculer la concentration Ca de l'atropine dans l'ampoule.
M(atropine) = 289,4 g / mol.
Ca= Cma / M(atropine) = 0,025 / 289,4 =8,6 10-5 mol / L.
Quantité de matière d'atropine : na = 8,6 10-5 x0,020 =1,7 10-6 mol.
On trouve également des ampoules de concentration Cb = 1,7 10-3 mol / L..
Q5. Calculer le volume de cette ampoule pour que la quantité de matière soit 1,7 10-6 mol.
1,7 10-6 = Cb V ; V = 1,7 10-6 / (1,7 10-3) =1,0 10-3 L ou 1,0 mL.
Etude
de l'extraction de l'atropine.
A
partir des feuilles de belladone, on isole une substance contenant du
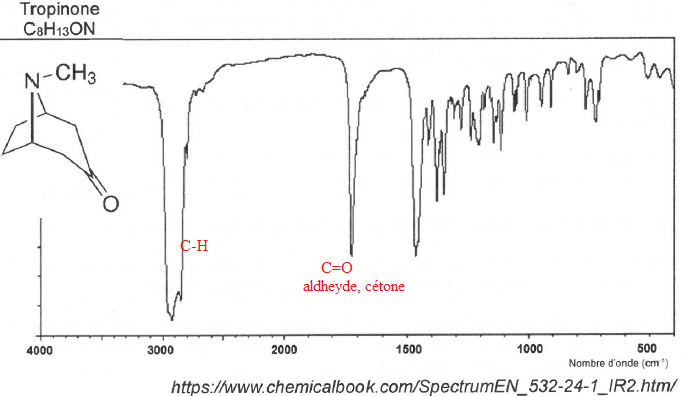
propanol, la tropinone et l'atropine. On réalise un spectre IR de l'une
de ces substances.
Q6. Identifier la substance.
Pas de large bande vers 3200 cm-1 : pas de fonction alcool.
Q7. Décrire le protocole expérimental de la CCM.
But : séparer et identifier les constituants d'un mélange.
Mise en oeuvre : placer l'éluant dans le bécher ( hauteur 5 mm), mettre un couvercle.
Sur la plaque CCM, tracer 2 traits au crayon de papier à 7 ou 8 mm des extrémités.
Sur le trait inférieur faire les dépots (pipette pasteur), espèces à analyser et substances étalon.
Placer la plaque dans le bécher, fermer, retirer dés que l'éluant atteint le trait supérieur.
3 Etude de la synthèse de l'atropine.
Dans la plante, la tropinone est réduite en tropanol à l'aide d'une enzymz TRI dite réductase.
Q8. Ecrire la demi-équation électronique du couple tropanol - tropinone.
C8H13ON +2H+ +2e- = C8H15ON
Q9.
En notant TRI / TRI-H le couple d'oxydoréduction de l'enzyme, établir
l'équation modélisant la transformation entre l'enzyme et la tropinone.
C8H13ON + 2TRI-H -->C8H15ON +2TRI.
|
...
|
....
|
Q10. Identifier et nommer les trois familles fonctionnelles présentes dans la molécule d'atropine.
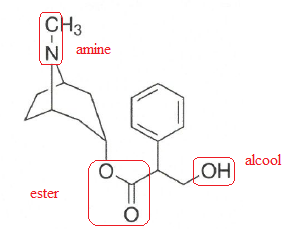
La synthèse résulte de la réaction entre l'acide tropique et le tropanol pour donner l'atropine.
Q11. Compléter l'équation de la réaction.
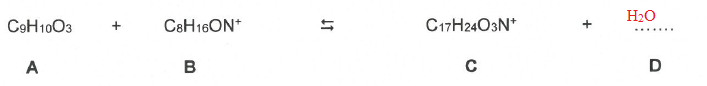
Q12 Citer deux intérëts du chauffage à reflux.
Le
chauffage à reflux permet d'accérer la réaction en travaillant à
température modérée, tout en évitant les pertes de matière : les
vapeurs se condensent dans le réfrigérant et retombent dans le ballon.
Q13. Indiquer le rôle de l'acide sulfurique.
Catalyseur.
On note nA, nB, nC et nD les quantités de matière à l'équilibre des espèces chimiques intervenant dans la transformation.
Q14. Exprimer la constante d'équilibre K à l'aide des quantités de matière.
K = nC nD /(nA nB).
Q15. Justifier l'effet d'éliminer l'eau au fur et à mesure de sa formation.
En éliminant l'eau au fur et à mesure de sa formation, on déplace l'équilibre dans le sens direct.
|
|
|
|