Partie n°1 : L’eau de Javel
Employée depuis plus de deux cents ans pour ses
propriétés blanchissantes et
désinfectantes, l’eau de Javel est un produit incontournable en France.
Cette solution
contient notamment des ions hypochlorite (CℓO
⁻(aq)) et
chlorure (Cℓ
⁻(aq)) dissous dans
l’eau. L’élément chlore se rencontre sous différentes formes : le
dichlore Cℓ
2, l’acide
hypochloreux HCℓO, l’ion chlorure Cℓ
⁻ et l’ion hypochlorite
CℓO
⁻.
1. Donner la
configuration électronique à l’état fondamental de l’atome de chlore.
Z = 17 : 1s
2 2s
2 2p
6 3s
2 3p
5.
2. Représenter le
schéma de Lewis de l’acide hypochloreux et du dichlore. On
précise que l’atome d’oxygène est central dans le schéma de Lewis de
l’acide
hypochloreux.
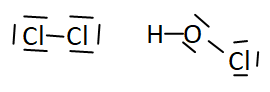 3.
3. Déterminer la
géométrie autour de l'atome d'oxygène dans la molécule d'acide
hypochloreux à l’aide de la méthode VSEPR et donner un ordre de
grandeur de
l’angle HOCl
AX
2E
2 : forme coudée en forme de V.
Du fait de la répulsion électronique entre les paires libres, l'angle
HOCl est inférieur à 109 °.
.
Les formes prédominantes de l’élément chlore en solution aqueuse
figurent dans le
diagramme potentiel-pH suivant pour une concentration totale des
espèces dissoutes égale à 0,1 mol·L
-1. On superpose au
diagramme la droite relative
au couple O
2 (g) / H
2O(l), tracée pour P
O2
= 1 bar
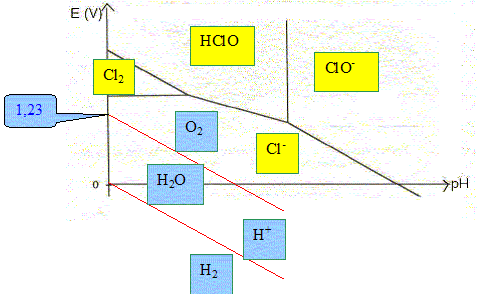
4. Dans le diagramme E-pH fourni, justifier la position des
domaines de stabilité de chaque espèce contenant du chlore, en s’appuyant
entre autres sur un calcul de nombre d’oxydation.
Cl
2 : n.o(Cl) = 0 ; Cl
- : n.o(Cl) = -1 ; ClO
- et HClO n.o(Cl) = +1.
En ordonnée : à pH fixé, plus le nombre d'oxydation est élevé, plus
l'espèce est oxydée et se trouve donc à potentiel plus élevé.
En abscisse : à pH faible HClO prédomine et à pH plus fort, ClO
- prédomine..
5. Justifier ue le dichlore est instable dans l'eau.
Le domaine de stabilité de Cl
2 est restreint à pH faible et
potentiel élevé. Un faible variation de pH ou de potentiel conduit à
une autre espèce chlorée. Le dichlore est donc thermodynamiquement
instable dans l'eau.
6. Montrer que la concentration des ions ClO
- aq d'une eau de Javel de titre 36°chl est de 1,607 mol / L.
36 L de dichlore ont été nécessaire pour préparer 1 L d'eau de Javel.
Volume molaire à 273 K sous 101,3 kPa : 22,4 mol / L.
36 / 22,4 = 1,607 mol / L.
Sur l'étiuette on lit : au contact d'un acide, un gaz toxique se dégage.
7. Justifier cette mise en garde.
ClO
-+Cl
-+2H
+ --> Cl
2 +H
2O. Dégagement de dichlore toxique.
Réaction de médiamutation ou antimutation, inverse de la dismutation.
8. Justifier le fait ue le dichlore est peu soluble dans l'eau.
L'eau est une molécule polaire pouvant former des liaisons hydrogèneet
le dichlore est une molécule apolaire ne pouvant former de liaisons
hydrogène.
Le dichlore est donc peu soluble dans l'eau.
9. Identifier les couples d'oxydoréduction dans l'équation 2ClO
- = O
2 + 2Cl
-.
ClO
- / Cl
- et O
2/H
2O.
2ClO- +4H++4e- = 2Cl- +2H2O.
2H2O= O2+4H++4e- .
Ajouter et simplifier.
10. Montrer que la
série de mesures proposées est compatible avec l'hypothèse d'un modèle
de vitesse d'ordre 2. En déduire la valeur de la constante de vitesse k.
t jours
|
0
|
50
|
100
|
150
|
200
|
250
|
300
|
[ClO-) mol / L
|
1,607
|
1,270
|
1,05
|
0,895
|
0,780
|
0,691
|
0,602
|
Dans le cas d'une cinétique d'ordre 2, le tracé 1 /[ClO
-] = f(t) doit être une droite. La constante de vitesse k est la pente de cette droite.
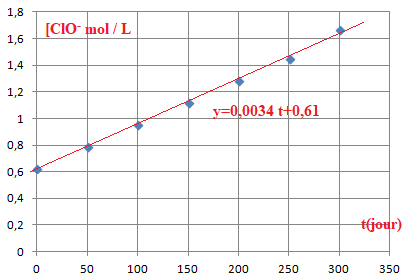
k= 0,0034 L mol
-1 jour
-1.
11. Nommer et donner la loi explicitant le lien entre température et constante de vitesse de réaction.
Loi d'Arrhénius : k(T) = A exp(-Ea/ (RT)).
12. Evaluer l'énergie d'activation de cette réaction.
A 25°C : k = 0,0027 ; à 30°C k = 0,0043 L mol
-1 J
-1.
k
1 / k
2 =
exp(-Ea/ (RT1)) / exp(-Ea/ (RT2)).
ln(k1 / k2 ) = Ea / R(1/T2-1/T1) ;
ln(27 / 43)=Ea / 8,314 (1/303-1/298).
-0,465 = Ea/8,314 x(-5,537) ; Ea = 69,9 kJ / mol.
Pour déterminer la concentration en ion hypochlorite d'un berlingot d’eau de Javel
ouvert depuis quelques temps, un titrage calorimétrique est effectué. Lors de ce titrage les ions hypochlorite CℓO
- (aq) sont
réduits par les ions iodure I
- (aq), en milieu basique. Les couples d’oxydoréduction mis
en jeu sont : CℓO⁻ (aq) / Cℓ⁻ (aq) et IO
3⁻ (aq) / I⁻ (aq).
13. Montrer que la réaction support de ce titrage est :
3CℓO
⁻ (aq) + I⁻ (aq) → 3Cℓ⁻ (aq) + IO
3⁻ (aq) (équation 3).
3 fois {ClO
-aq +2H
+aq
+ 2e---> Cl
- aq +H
2O}
I
-aq +3H
2O-->
IO3⁻ (aq) +6H+aq +6e-.
Ajouter et simplifier :3ClO-aq +I-aq --> 3Cl- aq + IO3⁻ (aq)
14. Calculer la constante d’équilibre de cette réaction à 298 K, commenter.
DG° 1= -2 F ln E°
ClO- / Cl-.
DG° 2= -2 F ln E°IO3- / I-.
DG° =3DG° 1-DG° 2=6 F E°IO3- / I- - 6E°ClO- / Cl-= -RT ln(K).
ln K = 6x96500( 1,73-1,08) / (8,314 x298)=151,9.
K est très grand, l'équilibre est très déplacé vers la formation des produits.
15. À partir des données thermodynamiques fournies, calculer l’enthalpie standard
de cette réaction à 298 K. Interpréter le signe de cette grandeur.
Loi de Hess :
DH° =3
DH
f° (Cl
-) +
DHf° (IO3-)-3
DHf° (ClO-)-DHf° (I-).
DH° =3*(-167,2)-221,3 -3x(-107,1)-(-55,2)= -346,4 kJ / mol.
La réaction est exothermique.
Les résultats obtenus sont récapitulés dans le graphique suivant. La
température initiale, notée
q0, vaut 25 °C.
16. Expliquer qualitativement l’allure de la courbe de titrage obtenue puis en
déduire la valeur du volume équivalent.
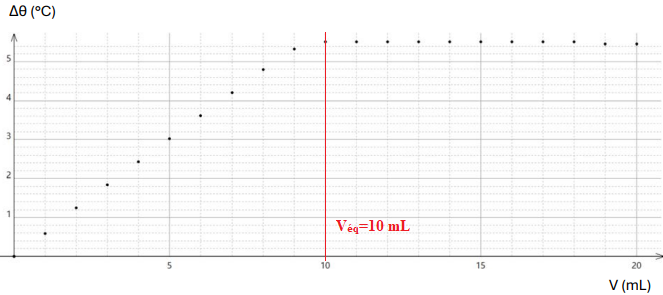
Avant l'éuivalence, les ions iodures sont consommés par les ions
hypochlorites ; la réaction étant exothermique, la température
augmente. Après l'équivalence, les ions hypochlorure sont en défaut et
les ions iodures en excès. Il n'y a plus de réaction et la température
reste constante.
,
17. Déterminer la concentration en ions hypochlorite de la solution du berlingot
ouvert.
3ClO-aq +I-aq --> 3Cl- aq + IO3⁻ (aq)
3 n(I-) = n(ClO-) ;
10 mL de solution d'ion iodure à 1,0 mol/ L a été introduit : n(ClO-) = 3 x0,01 = 0,03 mol.
Volume initial : 100 mL ; [ClO-] = 0,03*1000 / 100 = 0,3 mol / L.
Le berlingot a été dilué d'un facteur 3 : [ClO-]berlingot =0,9 mol / L.
18. En déduire la durée écoulée depuis l'ouverture de la bouteille d'eau de Javel en
supposant que celle-ci a été conservée à une température de 25 °C.
D'après le tableau ci-dessus, la durée est voisine de 90 jours.
La capacité thermique du calorimètre a été déterminée expérimentalement et est
évaluée à C
calo = 207 J·K
-1.
19. Proposer un protocole expérimental permettant de déterminer la valeur de la
capacité thermique du calorimètre.
Méthode des mélanges :
Mesurer un volume précis ( masse m
1) d'eau froide à la températue T
1. L'introduire dans le calorimètre.
Ajouter le même volume d'eau chaude à la température T
2. Repérer la température d'équilibre.
20. En utilisant le graphique et en considérant que la capacité thermique et la
masse volumique de la solution, tout au long du titrage, sont sensiblement
égales à celles de l’eau pure, évaluer l’enthalpie standard de la réaction de
titrage. Commenter.
Dq = 5,5 °C ; volume total V = 110 mL ; masse correspondante : m=0,11 kg.
m Ceau
Dq =0,11 x4185 x5,5 =2,5 kJ, valeur assez faible..