Le bismuth.
Concours
CAPES 2026.
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
.
| .. |
.
.
|
|
.
.
|
..
..
......
...
|
A. Radioactivité du bismuth 209.
Le bismuth est noté 20983Bi dans la
classification périodique.
Q1. Indiquer à quoi
correspondent les deux valeurs 209 et 83 associées à l’atome de bismuth.
209 :nombre de masse, nombre de nucléons, protons et neutrons ; 83 :
nombre de protons ( numéro atomique).
Pierre de Marcillac1 et ses collègues de l’Institut d’astrophysique
spatiale d’Orsay ont détecté fortuitement en 2003 la désintégration de
l’isotope 209 du bismuth. Cet atome était pourtant considéré comme
stable dans les tables les plus récentes des éléments périodiques. La
désintégration alpha du bismuth donne le thallium 205Tl.
Q2. Donner la
nature de la particule émise lors de la désintégration alpha.
Noyau d'hélium.
Q3. Proposer alors
l’équation de désintégration du bismuth 209.
20983Bi
--> 20581Tl
+42He
La constante de vitesse de désintégration, notée k, est de l’ordre de
1,093 × 10-27 s-1. On note N(t) le nombre
d’atomes de bismuth à l’instant t et N0 le nombre d’atomes à
l’instant initial de l’étude.
Q4. Exprimer N(t)
en fonction des données de l’énoncé et de N0.
N(t) = N0 exp(-kt)
Q5. Définir et
calculer le temps de demi-vie du bismuth 209. Commenter en relation
avec la découverte très récente de sa radioactivité.
Temps de demi-vie : durée au bout de laquelle la moitié des noyaux
initiaux se sont désintégrés.
½N0 = N0 exp (-1,093 10-27 t½).
0,5 =exp (-1,093 10-27
t½); ln(0,5) = - ln(2) = -1,093 10-27 t½;
t½ =6,34 1026 s ou 2,0 1019 ans.
Sa très longue période radioactive fait du bismuth un élément à la
radioactivité infime, demeurée inaperçue jusqu'au début du XXI e
siècle.
B. Obtention du bismuth /
métallurgie.
Le bismuth est un sous-produit de l’industrie de plomb par le procédé
Betts. Le plomb est obtenu à partir de sulfure de plomb, mais de
manière impure et il contient beaucoup d’autres métaux dont le bismuth.
Le procédé Betts consiste à couler le plomb d’oeuvre, après décuivrage
et désétamage, sous forme d’anodes de 200 kg. La cathode est en plomb
de 2 mm d’épaisseur. L’électrolyte est une solution concentrée d’acide
fluosilicique (2 H+(aq), SiF62-
(aq)) contenant 85 g ⋅ L-1 de plomb (II). La surface de la
cathode en contact avec l’électrolyte est environ égale à un mètre
carré. On réalise alors l’électrolyse pendant trois jours, à 40-50 °C
et sous 0,4 à 0,6 V, avec une densité de courant de 250 A ⋅ m-2.
Q6. Indiquer les
trois ions présents majoritairement dans l’électrolyte.
H+(aq), SiF62-(aq))
; Pb2+aq .
Pour simplifier, on modélise cet électrolyseur par une anode impure
contenant du plomb et du bismuth et une cathode en plomb pur, trempant
dans l’électrolyte précédent. On assimile le potentiel rédox du couple
Bi2+(aq)/Bi(s) à sa valeur standard 0,290 V. La réduction
des ions H+(aq) n’est pas considérée ici pour des raisons
cinétiques.
Q7. Calculer le
potentiel rédox du couple Pb2+(aq)/Pb(s) dans le milieu.
[Pb2+aq] = 85 / 207=0,41 mol / L.
E = E°(Pb2+/Pb(s) +0,06 / 2 log ( [Pb2+]= -0,126
+0,03 log (0,41) = -0,138 V.
Q8. Identifier
l’oxydant le plus fort et le réducteur le plus fort présents dans le
système et écrire à chaque électrode les demi-équations qui ont lieu.
Conclure sur la réaction de fonctionnement de l’électrolyseur.
Le réducteur le plus fort s'oxyde à l'anode soluble : Pb(s)
= Pb2+aq +2e- .
L'oxydant le plus fort se réduit à la cathode : Pb2+aq +2e-
= Pb(s).
Bilan : Pb(s)anode
= Pb(s)cathode .
Q9. Faire un schéma
de l’électrolyseur en indiquant la polarité, le nom des électrodes et
le sens de circulation des différents porteurs de charge. Le procédé
s’appelle « à anode soluble ».
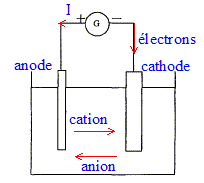
Q10. Expliquer
cette dénomination et indiquer sous quelle forme le
bismuth est récupéré en fin d’électrolyse.
Le plomb de l'anode disparaît et le bismuth se retrouve dans les boues
anodiques.
Q11. Déterminer la
charge
totale qui circule dans l’électrolyseur durant les trois jours. Montrer
que l’anode n’est pas entièrement consommée au bout des trois jours
d’électrolyse.
Q = I t = 250 x3 x24 =1,8 104 Ah ou 1,8 104 x3600 =6,48 107 C.
n(Pb(s) = Q / (2F) =6,48 107 / (2*96500)=335,75 mol.
Masse de plomb = 335,75 x207=6,95 104 g=69,5 kg.
Au bout de 3 jours l'anode de 200 kg n'est pas entièrement consommée.
Le bismuth se retrouve dans les boues anodiques. La
phase métallique, obtenue après des traitements non étudiés, renferme
le bismuth en présence d’un peu de plomb. Cette phase métallique est
alors traitée, en présence d’air, dans un four à coupellation dont la
température est d’environ 1000 °C. Le bismuth est alors récupéré sous
forme d’oxyde Bi2O3(l).
Q12. Écrire la réaction
d’obtention de
l’oxyde de bismuth à partir du bismuth dans les conditions de
température du four à coupellation, en ajustant le coefficient
stoechiométrique de l’oxyde de bismuth à 1. On notera cette réaction
[a].
2Bi(s ) + 1,5O2 (g) --> Bi2O3(l).
Q13.
Justifier la valeur nulle pour les enthalpies standard de formation du
dioxygène gazeux et du bismuth solide à 25 °C.
Les éléments sont dans leur forme la plus stable, état standard, dans les conditions
standard.
Q14.
Déterminer l’enthalpie standard de réaction et l’entropie standard de
réaction associées à la réaction [a].
DrH°298=DfH°298(Bi2O3)-2DfH°298(Bi(s))
-1,5 DfH°298(O2(g))=DfH°298(Bi2O3)= -573,9 kJ/mol.
DrS°=S°(Bi2O3(l))
-2S°(Bi(s)) -1,5 S°(O2(g))=177,6
-2*56,8-1,5*205,0= -243,7 J mol-1 K-1= -0,2437 kJ mol-1 K-1.
Dans le
cadre de l’approximation d’Ellingham, on considère que les enthalpies
standard et entropies standard de réaction sont indépendantes de la
température, en dehors de tout changement de phase. On fait également
l’hypothèse que les liquides présents dans le milieu sont non miscibles
et que la pression partielle du dioxygène dans l’air est égale à 0,2
bar. Q15. Déterminer
l’enthalpie libre de réaction de la réaction [a] à 1000 °C. Conclure
quant au carac-tère spontané ou non de la réaction [a] dans les
conditions envisagées.
DrG°=DrH° -T DrS°=-573,9
+1273 x 0,2437= -263 kJ mol-1, valeur négative, la réaction
est spontanée dans le sens direct.
Q16. Détailler les raisons du choix
de la température modérée de 1000 °C pour cette réaction [a].
La temprature doit être supérieure à la température de fusion ( 817 °C) de Bi2O3.
DrH° < 0 et -T DrS°> 0. Au-delà de 1726°C, la réaction n'est plus spontanée.
A 1000°C Bi et Bi2O3 sont liquides, cela augmente la surface de contact avec le dioxygène, donc la vitesse de la réaction.
Chauffer entre 1000 °C et 1726 °C a peu d'intérêt et nécessite une dépense énergétique.
. Le bismuth est finalement obtenu à partir de l’oxyde Bi2O3
par réduction.
|
.
|
....
|
C.
Utilisation du bismuth(0) en chimie organique.
Le
bismuth (0) peut être utilisé dans la synthèse du diosphénol (molécule
D2) qui est un terpénoïde présent dans l’huile essentielle de Buchu3.
La figure suivante présente la synthèse à partir du (-)-menthol.
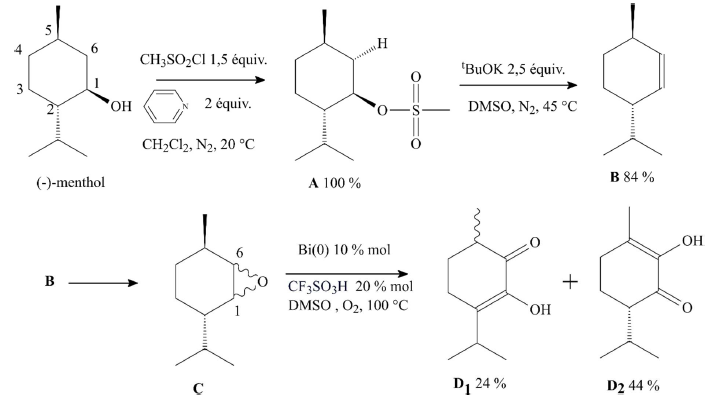
Q17. Indiquer la
grandeur à laquelle fait référence le signe (-) qualifiant le menthol.
Proposer un appareil pour déterminer cette grandeur.
Une
molécule levogyre ( signe (-)) a la propriété de faire dévier le plan de
polarisation de la lumière polarisée vers la gauche d'un observateur
qui reçoit la lumière.
Une molécule levogyre est notée avec un (-) devant sa nomenclature. Le pouvoir
rotatoire, déterminé expérimentalement, est négatif.
Le polarimètre mesure cette grandeur.
Q18.
Préciser, en justifiant, le descripteur stéréochimique du carbone 1 de
la molécule de (-)-menthol.
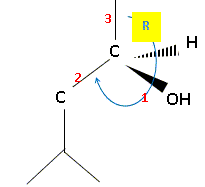
Le groupe mésylate -OSO2CH3 pourra être noté -OMs
par la suite. L’étape permettant le passage de A à B utilise le
tertiobutylate de potassium en excès qui joue le rôle de base forte
dans le solvant diméthylsulfoxyde DMSO.
Q19. Proposer un
mécanisme limite pour l’obtention du composé B à partir de A et
expliquer la régiosélectivité de la réaction.
Le carbone n°2 porte un groupe très encombrant, contrairement au carbone n° 6.
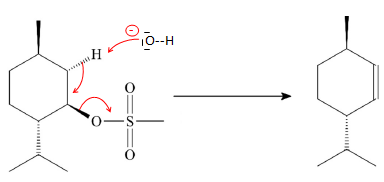
Q20. Expliquer
l’intérêt de la transformation du groupe hydroxyle du (-)-menthol en
groupe mésylate.
Le groupe mésylate est un groupe partant ( car il est très
stable) bien meilleur que le groupe OH.
Q21. Proposer un
réactif en explicitant sa structure pour former l’époxyde C.
Faire réagir l'alcène avec un peracide obtenu par action de l'eau oxygénée sur un acide carboxylique.
L'acide méta-chloroperbenzoïque.
Lors de la dernière étape, le bismuth est utilisé comme catalyseur afin
d’obtenir les isomères D1 et D2.
Q22. Calculer la variation des nombres d’oxydation des carbones
numérotés 1 et 6 lors de la dernière étape de la synthèse pour passer de C à D2. En
déduire la nature de cette étape.
Carbone n°1 : le nombre d'oxydation du carbone passe de 0 à II : oxydation.
Carbone n° 6 : le nombre d'oxydation du carbone passe de 0 à I : oxydation..
Lors de cette étape, l’acide triflurométhanesulfonique est utilisée. Les pictogrammes de sécurité sui-vants y sont associés :
Q23. Donner un adjectif associé à chacun de ces pictogrammes et les précautions à prendre.

Port de gants, blouse, travail sous hotte.
Utilisation du bismuth III en chimie organique.
Le bismuth au degré d’oxydation (III) peut être utilisé comme acide de
Lewis dans de nombreuses réactions. Le bismuth se trouve dans la
quinzième colonne et sur la sixième période de la classification
périodique.
Q24. Préciser la
configuration électronique de valence du bismuth dans son état
fondamental et justifier la stabilité du degré d’oxydation (+III).
[Xe] (4f)14 (5d)10 (6s)2 (6p)3.
En perdant 3 électrons, l'ion résultant possède une couche de valence saturée.
Q25. Définir un acide de Lewis et donner un exemple d’acide de Lewis utilisé comme catalyseur (autre que le bismuth).
Un acide de Lewis est une molécule ou ion qui peut accepter une paire d'électrons.
AlCl3 est un acide de Lewis.
La molécule BG9719, antagoniste des récepteurs de l’adénosine A1,
est utilisée dans le traitement des thérapies rénales. BG9719 peut être
synthétisée à partir de l’acide
(2R,3R)-bicyclo[2.2.1]hept-5-ene-2,3-dicarboxylique (figure
ci-dessous). Sa synthèse diastéréosélective peut être menée à partir du
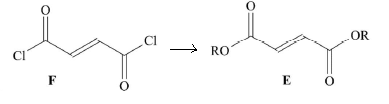
menthol et de dichlorure de l’acide fumarique F et est présentée sur la
figure suivante.
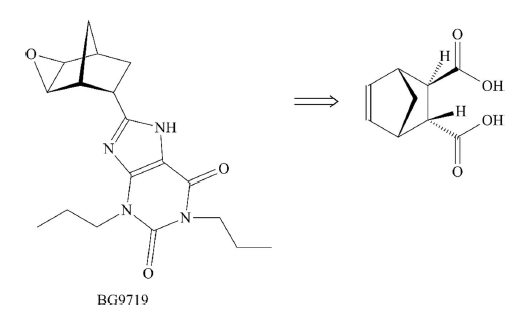
On étudie tout d’abord l’obtention du diester E. On notera R le groupe (+)-menthyl pour simplifier les structures.
Q26. Proposer un
mécanisme pour l’obtention du composé E à partir du dichlorure de
l’acide fumarique F dans la pyridine. On pourra simplifier
judicieusement toute structure pour alléger l’écri-ture du mécanisme.
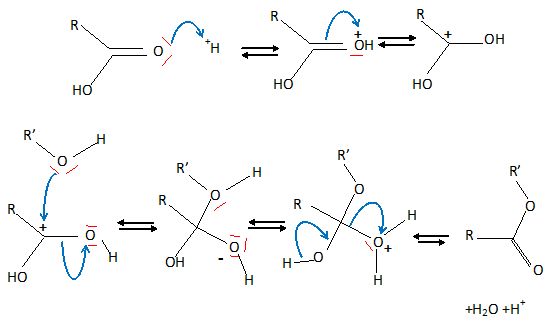
Lors de l’étape suivante de la synthèse, la réaction de Diels-Alder est
menée en présence de chlorure de bismuth dans le toluène pour obtenir H
à partir de E purifié. Le chlorure de bismuth joue ici un rôle de
catalyseur.
On définit l’excès diastéréomérique de comme étant la valeur absolue de
la différence entre les quantités relatives des deux diastéréoisomères
produits dans une réaction :
de = |P1-P2| / (P1+P2).
Q27. Donner un réactif G adapté pour obtenir H par la réaction de Diels-Alder.
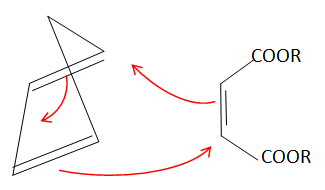
Un autre composé minoritaire H’ est obtenu lors de cette étape.
Q28.
Représenter H’ et indiquer sa relation d’isomérie avec la molécule H.
Calculer la quantité relative de chacun deux isomères H et H’.
Commenter.
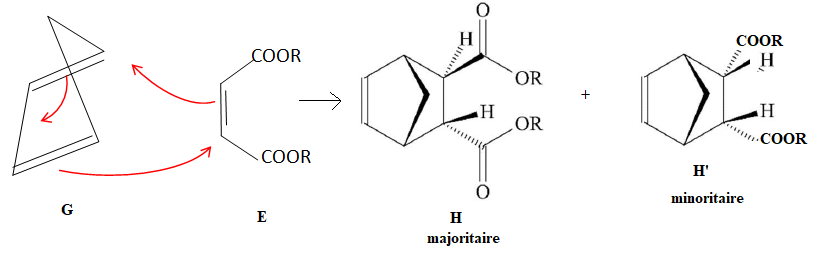
H et H' sont des diastéréoisomères.
de(H)=0,04.
On note x la quantité de H et 1-x celle de H'
0,04 = |x-(1-x| = 1 ; 0,04 = 2x-1 ; x = 1,04 / 2 = 0,52 ( 52 %).
Le composé endo est obtenu le plus rapidement ; si on laisse la
réaction se prolonger longtemps, l'équilibre est en faveur du composé
exo.
La réaction est peu diastéréosélective.
Le produit H a été caractérisé par RMN 1H (CDCl3,270
MHz) et présente, entre autres, deux signaux caractéristiques à 6,25
ppm (doublet dédoublé, 1H) et à 6,05 ppm (doublet dédoublé, 1H).
Q29. Attribuer les deux signaux, autant que possible, et justifier leur multiplicité.
Doublet de doublet : proton de la double liaison C=C : les carbones voisins portent chacun un proton.
Lors de la dernière étape, on forme à partir de H l’acide carboxylique souhaité.
Q30. Proposer une
ou plusieurs étapes de synthèse et les conditions opératoires associées
pour l’ob-tention de l’acide carboxylique I à partir de H.
Saponification de l'ester : H est mis dans une solution contenant de l'eau et de la soude.
Q31. Expliquer l’intérêt
de l’utilisation du (+)-menthol dans cette synthèse.Le (+) menthol joue
le rôle d'auxiliaire chiral guidant la réaction vers la formation de le
diastéréoisomère désiré.
Utilisation en pharmacologie.
Le sous-salicylate de bismuth est utilisé comme médicament pour soulager les malaises gastriques et les diarrhées.
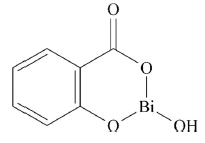
On se propose de déterminer la masse de bismuth dans un comprimé de
Pepto Bismol par un titrage complexométrique avec l’EDTA. La notice du
médicament indique 262 mg de bismuth par comprimé. Le protocole de
dosage ci-dessous est proposé :
Un comprimé de masse 1,180 g est écrasé dans un mortier. On
introduit 0,150 g de la poudre obtenue dans un erlenmeyer de 250 mL
dans lequel on ajoute 10 mL d’acide nitrique à 0,5 mol⋅L-1.
Après avoir homogénéisé le mélange, on ajoute 40 mL d’eau distillée et
on porte le mélange à ébullition pendant 15 minutes. On transvase
quantitativement le contenu dans une fiole jaugée de 100 mL et on
ajuste au trait de jauge avec de l’eau distillée. On appelle S la
solution ainsi obtenue. Cette solution S est finalement titrée par une
solution d’EDTA de concentration C=0,0100 mol⋅L-1 en
présence d’orangé de xylénol qui sert d’indicateur coloré. Le volume
équivalent obtenu est de 15,9 mL. Lors de la mise en solution en milieu
acide, on admet que le sous-salicylate de bismuth est transformé de
manière quantitative en ion Bi3+ et en acide salicylique. De plus, l’acide nitrique ajouté est en large excès par rapport au sous-salicylate de bismuth. Q
32. Calculer le pH de la solution S, avant qu’elle ne soit titrée.
Concentration de l'acide nitrique dans la fiole jaugée C = 0,5 x 10 / 100=0,05 mol / L.
pH = - log (C)=- log (0,05) = 1,3.
Q33. Tracer le
diagramme de prédominance en pH du ligand EDTA. Conclure sur la forme
prédominante de ce ligand dans le domaine de pH utilisé dans le
protocole.
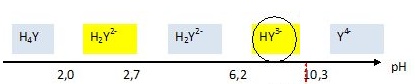
A pH = 1,3, la forme H4Y prédomine.
Q34. En s’appuyant
sur les données fournies, écrire l’équation de la réaction support du
titrage et calculer sa constante d’équilibre. Conclure.
Bi3+ + H4Y = BiY-+4H+.
K = [BiY- ] [H+]4 / ([Bi3+][H4Y]).
On donne ß = [BiY- ]c° / ([Bi3+] [Y4- ]) avec log ß = 27,8.
K = ß [H+]4 / [H4Y].
Ka1 = 10-2=[H3Y-] [H+] / [H4Y] ; Ka2 = 10-2,7=[H2Y2-] [H+] / [H3Y-] ;
Ka3 = 10-6,2=[HY3-] [H+] / [H2Y2-] ; Ka4 = 10-10,3=[Y4-] [H+] / [HY3-] .
Ka1 Ka2 Ka3 Ka4=[H+]4[Y4-] / [H4Y] =10-21,2.
K =ß Ka1 Ka2 Ka3 Ka4 .
K = 1027,8 x10-21,2 =106,6.
K étant grand, la réaction est favorisée quantitativement, ce qui est attendu pour une réaction de titrage.
L’orangé de xylénol est utilisé ici comme indicateur coloré. Sa
structure est fournie . En solution acide (pH inférieur à 6,7), il
possède un maximum d’absorption autour de 435 nm. Les complexes formés
avec l’ion Bi3+ sont de couleur rouge à violacée.
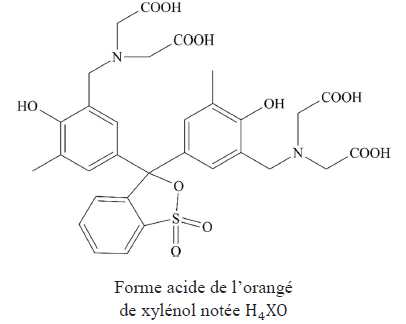
Q35. Indiquer la
couleur de l’orangé de xylénol en solution acide en absence d’ion
bismuth, puis en présence d’ions bismuth et expliquer le changement de
couleur attendu lors du dosage.
L'orangé de xylénol absorbe dans le bleu ; sa couleur, complémentaire du bleu, est l'orangé.
En présence d'ion bismuth il est rouge violacé.
Avant l'équivalence, Bi3+ est en excès, la solution est rouge violacé.
Après l'équivalence, l'ion Bi3+ est en défaut : la solution est orangé.
L’incertitude-type u(m) sur la masse de bismuth déterminée par le
titrage d’un comprimé complet est estimée par une simulation
Monte-Carlo codée en langage Python. L’exécution du script renvoie :
u(m) = 3,3134715376757486 mg.
Q36. Exploiter le
titrage pour déterminer la masse de bismuth dans un comprimé complet.
Présenter le résultat muni de son incertitude-type. Comparer avec les
données fournies par la notice du médicament.
A l'équivalence : [Bi3+] V = CH4Y Véq ; [Bi3+] = CH4Y Véq / V =0,010 x 15,9 / 100= 1,59 10-3 mol / L.
masse m = [Bi3+] MBi V = 1,59 10-3 x 209 x 0,100=3,32 10-2 g dans 0,15 g de comprimé.
Soit dans un comprimé complet de 1,18 g :3,32 10-2 x 1,18 / 0,15 = 0,261 g.
Soit 261±3 mg.
On réalise un z score : z = |261-262| / u(m) = 1 / 3,3 =0,30 < 3.
Le titrage fournit une masse de bismuth compatible avec la notice.
|
|
|
|