Physique chimie : Traitement de l'eau d'une
piscine. Concours
CAPLP maths sciences 2025.
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
.
| .. |
.
.
|
|
.
.
|
..
..
......
...
|
.Traitement de l’eau de piscine par électrolyse de sel.
L’électrolyse de sel permet de nettoyer l’eau d’une piscine en la
désinfectant. Les ions chlorure apportés par le sel se transforment en
espèces chlorées grâce à l’apport d’énergie électrique.
Le diagramme potentiel-pH du chlore en solution aqueuse est donné. La concentration de tracé est C=0,100 mol∙L−1 pour l’ensemble des espèces chlorées en solution aqueuse et la pression partielle de tracé en dichlore gazeux est de 1,00 bar.
24. Identifier les espèces A, B, C, D parmi Cl−(aq),Cl2(g), HClO(aq) et ClO−(aq).
25. Déterminer le pKa du couple HClO(aq) / ClO−(aq).
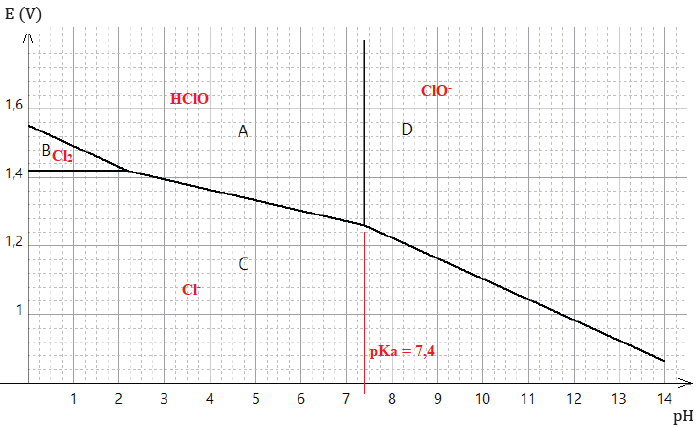
26. Montrer que la droite frontière séparant les domaines O2(g) et H2O(l),
pour une pression en dioxygène de 1 bar et à 25 °C, a environ pour
équation : E=1,23−0,06 pH (en volts). Tracer cette droite et y préciser
le domaine de stabilité de l’eau.
E° (
O2(g) / H2O) = 1,23 V ;
O2 +4e- + 4H+ =
2H2O
E3 = E° (
O2(g) / H2O) +0,015 log
([H+]4
P2O2)
E3 = 1,23 +0,06
log [H+] =
1,23 -0,06
pH.
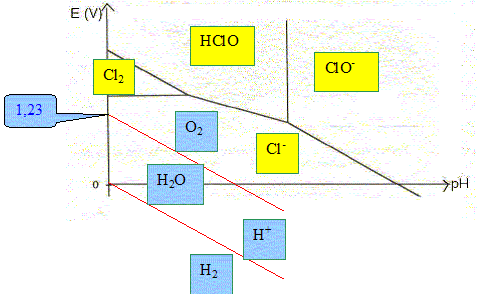 27. Conclure quant à la stabilité thermodynamique du dichlore gazeux dans l’eau d’une piscine.
27. Conclure quant à la stabilité thermodynamique du dichlore gazeux dans l’eau d’une piscine.
Le dichlore ghazeux n'est pas stable dans l'eau d'une piscine. Il est réduit en ion chlorure.
Principe de l’électrolyse de sel.
28. Ecrire la demi-équation d’oxydoréduction se produisant à l’anode de la cellule d’électrolyse.
Oxydation des ions chlorure en dichlore.
2Cl-aq --> Cl2(g) + 2e-.
29. Ecrire la demi-équation d’oxydoréduction se produisant à la cathode de la cellule d’électrolyse.
Réduction de l'eau.
2H2O +2e---> 2HO- aq+H2(g)
30. Montrer que l’équation de la réaction de l’électrolyse est :
2Cl-aq +2H2O +2e---> Cl2(g) + 2e-+2HO- aq+H2(g).
Simplifier : 2 H2O(l) + 2 Cl−(aq) ⇄ Cl2(g) + 2 HO−(aq) + H2(g) (1)
Données :
– Masse molaire du chlore : M(Cl) = 35,5 g ∙ mol−1.
– Intensité du courant dans une cellule d’électrolyse : I = 18 A.
31. Calculer la masse de dichlore produite par une cellule d’électrolyse par heure.
Q = I t = 18 x 3600 =64 800 C.
64800 / 96500 =0,67 mol d'électrons..
0,67 / 2 =0,336 mol de dichlore.
Masse de dichlore : 0,336 x(35,5 *2) = 23,8 g.
Les ions hydroxyde et le dichlore formés au cours de l’électrolyse sont
consommés lors d’une nouvelle transformation chimique d’équation :
Cl2(g) + 2 HO−(aq) ⇄ ClO−(aq) + Cl−(aq) + H2O(l) (2)
32. Donner le nom de ce type particulier de réaction électrochimique.
Le dichlore se dismute en ions chlorure et hypochlorite.
|
...
= =
|
....
|
Procédé de production de dichlore in situ par électrolyse de sel
Dans le souci d’améliorer l’aspect écologique du traitement de
l’eau et la sécurité du personnel, on souhaite équiper le bassin
sportif du centre aquatique d’un électrolyseur de sel qui produit du
dichlore in situ, dans un local technique.
Données :
– Intensité du courant dans une cellule d’électrolyse :I= 18 A.
– Tension aux bornes d’une cellule d’électrolyse : U = 10,8 V.
– Conductivité de la solution salée traversant la cellule d’électrolyse : s = 3,0 S ∙ m−1.
– Surface d’une électrode de cellule d’électrolyse : S = 0,010 m2.
– Distance entre deux électrodes d’une cellule unité d’électrolyse : e = 6 mm.
Des cellules d’électrolyse composées de plusieurs électrodes
Dans l’objectif d’augmenter la production de dichlore, les cellules
d’électrolyse de l’électrolyseur sont composées de plusieurs
électrodes. Si une électrode est insérée entre l’anode et la cathode de
la cellule d’électrolyse, elle se polarise sur chaque face. On obtient
ainsi plusieurs cellules
unités disposées à la suite les unes des autres.
33. Calculer la résistance électrique de la solution comprise entre les deux électrodes d’une cellule unité d’électrolyse.
Conductance G = sS / e =3,0 x 0,010 / (6 10-3) =5 siemens.
R = 1/ G =1 /5 = 0,2 ohm.
Les cellules unités constituant la cellule d’électrolyse peuvent être
modélisées par des résistances électriques montées en série.
34. En déduire le nombre d’électrodes de la cellule d’électrolyse utilisée pour le bassin sportif du centre aquatique.
Rcellule = U / I = 10,8 / 18=0,6 ohm.
Nombre d'électrodes : 0,6 / 0,2 = 3.
Choix du nombre de cellules de l’électrolyseur.
La gamme d’électrolyseurs industriels choisie permet une production de Cl2(g) de 3,9 g∙h−1∙A−1. Pour le bassin sportif, le fabricant conseille une production optimale de dichlore égale à 560 g∙h−1.
35. Calculer le nombre de cellules d’électrolyse à disposer en parallèle dans l’électrolyseur pour assurer cette production.
3,9 x18 =70,2 g h-1.
Nombre de cellules :n =560 / 70,2 ~ 8.
36. En déduire la puissance consommée par l’électrolyseur.
n I U = 8 x 18 x10,8 =1,5 103 W.
Ventilation du local technique et adoucissement de l’eau.
37. Expliquer pourquoi il est nécessaire de ventiler le local technique où se trouve l’électrolyseur.
Le dichlore est toxique pour les yeux, la peau et les poumons.
38. Expliquer l’intérêt d’utiliser un adoucisseur d’eau en amont du procédé d’électrolyse.
Elimination du calcaire présent dans l'eau.
|
|
|
|