Luminosité sous-marine
La vision sous-marine est directement impactée par la pénétration de la lumière dans les profondeurs marines,
elle-même dépendant fortement de la longueur d'onde. En effet, les molécules d'eau absorbent une certaine
partie du rayonnement électromagnétique.
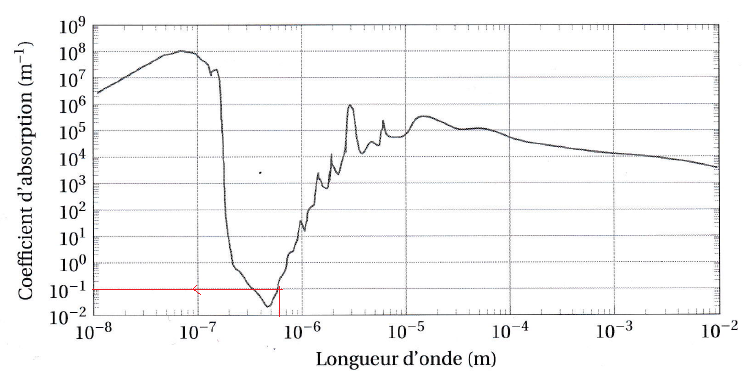
Le coefficient d'absorption correspond au rapport de l'absorbance d'une
solution sur la longueur du chemin optique suivi (source : https : /
/fr.wikipedia .org/wlki/Fichier:Absorption-spectrum-of - liquid_water.
png).
L'absorption des molécules d'eau est due à différents phénomènes correspondant à des transitions énergéüques
différentes. Celles-ci sont répertoiiée dans le tableau ci-dessous.
|
Type de transition |
Gamme d'énergie |
électronique
|
>3,2 eV
|
vibrationnelle
|
de 3,2 à 0,25 eV
|
rotationnelle
|
< 0,25 eV
|
Q24 . Calculer l'énergie associée à la bande transmise présente à 500 nm = 5 10-7 m sur le spectre d'absorption de l'eau.
E = h c / l ; célérité de la lumière dans l'eau c = 2,2 108 m /s.
E = 6,63 10-34 x2,2 108 / (5 10-7)=2,9 10-19 J ou 2,9 10-19 /(1,6 10-19) =1,8 eV.
Coefficient d'absorption 0,10 m-1.
Q25. Sélectionner le type de transition par laquelle l'eau absorbe les rayonnements visibles du spectre.
Transition vibrationnelle.
Q26. À partir du spectre d'absorption de l'eau, déterminer les radiations lumineuses qui pénètrent le plus en
profondeur l'eau des océans. Justifier.
Les radiations bleues et UV pénètrent le plus aux grandes profondeur ( coefficient d'absorption élevé).
La lumière pénétrant.les profondeurs impacte directement la vie
sous-marine notamment végétale. Plusieurs types d'algues existent selon
les profondeurs sous-marines. On propose de comparer les algues vertes
et rouges dont la composition en pigment est donnée ci-dessous :
Verte :
Chlorophylle a et b, carotène
Rouge :
Chlorophylle a, carotène, phycoérythrine, phycocyanine.
La üvie végétale sous-marine est notamment conditionnée par la
photosynthèse. La photosynthèse est une étape primordiale de la vie des
plantes, qui nécessite l'absorption d'un maximum de lumière par des
pigments. Parmi ces pigments on peut citer les chlorophylles, les
caroténoïdes (regroupant les carotènes et les xanthophylles), la
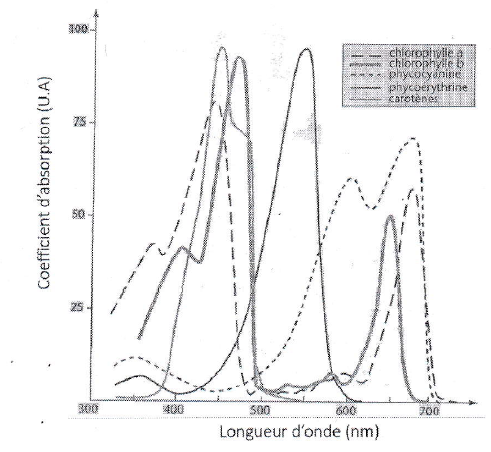
phycoérythrine et la phycocyanine. Les spectres d'absorption de ces
différents pigments sont donnés.
 Q27
Q27. Justifier la couleur des algues vertes.
Les algues vertes contiennent un pigment vert appelé chlorophylle
Q28. À partir des figures, préciser le type d'algue dont I'abondance est plus marquée au fond de l'océan.
Les algues dont le pigment lui permet d'absorber la lumière bleue
capable de pénétrer profondément dans l'océan : les algues rouges.
S'éclairer au fond de l'océan
Pour s'éclairer au fond de I'océan, les plongeurs ont recours à des
bâtons lumineux pour compenser le manque de luminosité en profondeur
mais aussi la perte de certaines couleurs comme vu précédemment. Les
bâtons
les plus utilisés reposent sur le principe de chimiluminescence qui
permet d'avoir une lumière intense sur un temps assez long (jusqu'à
plusieurs heures) sans source électrique.
La chimiluminescence repose sur l'émission de lumière par fluorescence d'une molécule, appelée photochrome.
Cette molécule passe de son état fondamental à un état excité par
absorption d'énergie produite par une réaction chimique (d'où le terme
chimi-luminescence). Ce photochrome va alors se désexciter en
produisant de la lumière, dont la longueur d'onde varie selon le
photochrome utilisé.
La réaction chimique ayant lieu dans les bâtons luminenx repose souvent sur la molécule d'oxalate de diphényle.
lll.2.1 Synthèse de l'oxalate de diphényle.
On donne les formules des molécules intervenant dans la synthèse étudiée.
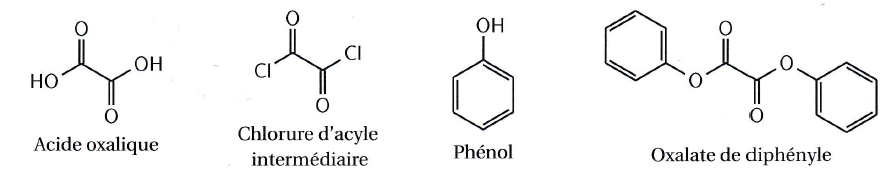
Le protocole de la synthèse de l'oxalate de diphényle est donnée
ci-dessous. Elle débute par la formation d'un chlorure d'acyle à partir
d'acide oxalique puis une étape d'estérification avec du phénol permet
de former la molécule souhaitée.
Étape 1 : Formation du chlorure d'acyle intermédiaire
Dans un environnement parfaitement sec mettre de l'acide oxalique (1,2
g) dans du toluène dans un ballon plongé dans un bain de glace
(travailler sous une hotte).
On ajoute par petites quantités du chlorure de thionyle SOCI
2
(en excès). Une fois l'ajout terminé, la réaction est maintenue à
température ambiante durant une heure. Au cours de la réaction, deux
gaz sont produits.
On ne détaille pas ici les traitements de la réaction qui ont permis de récupérer le chlorure d'acyle intermédiaire.
Étape 2: Estérification
On dissout le phénol (3,0 g) et de la triéthylamine N(CH
3)
3 (en excès) dans du toluène.
On refroidit cette solution dans un bain de glace puis toujours en
milieu sec on ajoute le chlorure d'acyle intermédiaire par petites
fractions.
Un précipité se forme immédiatement après l'ajout du chlorure d'acÿe,
c'est de l'oxalate de diphényle. Il faut chauffer à reflux pendant 30
minutes.
On refroidit la solution dans un bain de glace et on filtre sous vide
pour récupérer les cristaux. Les étapes de purification de l'oxalate de
diphényle ne sont pas précisées ici. On obtient 2,8 g d'oxalate de
diphényle.
Q29. Proposer une nomenclature offlcielle pour l'acide oxalique de départ.
Acie éthanedioïque.
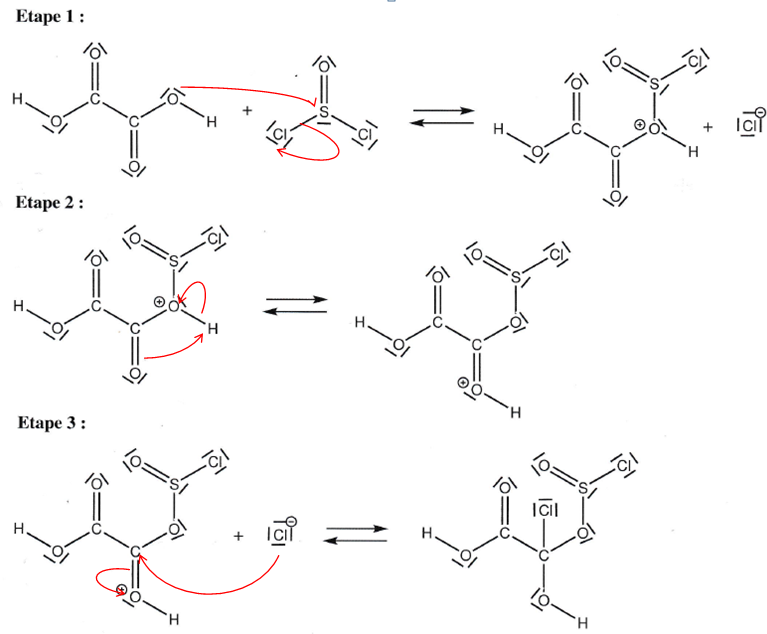
Q30. Le mécanisme
de la première étape est proposé. Compléter le mécanismee en
représentant les flèches courbes de chacun des actes élémentaires.
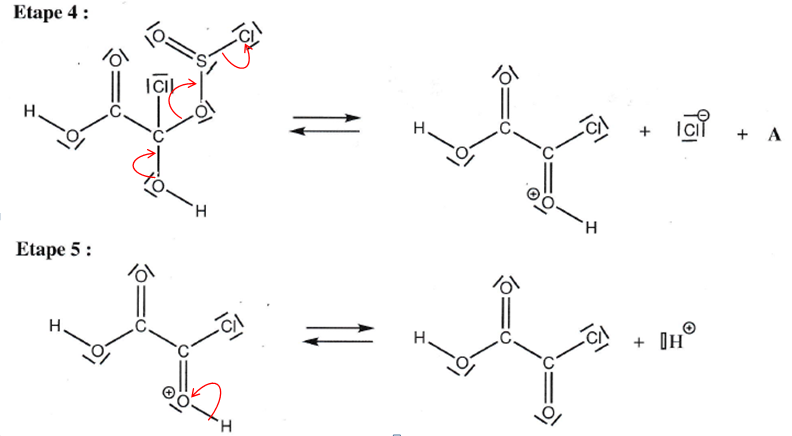 Q31
Q31. Déterminer la formule brute du composé A formé lors de la quatrième étape de ce mécanisme.
SO
2.
Q32. À I'aide du mécanisme donner l'équation-bilan de la première étape de la synthèse. Identifier
alors les deux gaz formés au cours de cette étape.
HOOC-COOH +SOCl
2 --> HOOC-COCl +SO
2+HCl.
,
Q33. La seconde étape de cette synthèse fait intervenir de la triéthylamine. Identifier la principale propriété
chimique de ce composé. Identifier alors la molécule suscepüble de réagir avec ce composé au cours de la
seconde étape. Iustifier.
La triéthyle amine est basique et nucléophile. Elle réagit avec le chlorure d'acyle.
Q34. Proposer une explication quant à l'introduction des réactifs dans un bain de glace lors de l'étape 2 de la
synthèse alors que la suite de la réaction s'effectue grâce à un montage à reflux.
La réaction entre la triméthyle amine et le chlorure d'acyle est exothermique.
Q35. Justifier que la formation de I'oxalate de diphényle peut être suivie par spectroscopie infrarouge.
L'oxalate de diphényle possède un grand nombre de double liaisons et de doublets électroniques libres conjugués.
Q36. Déterminer le rendement de la synthèse de l'oxalate de diphényle par cette voie.
Acide oxalique + 2 phénol --> oxalate de diphényle + 2H
2O.
M(acide oxalique) = 2*(12+32+1)=90 g/mol
n(acide oxalique) =1,2 /90=0,0133 mol.
M(phénol) = 94 g / mol.
n(phénol) = 3,0 / 94 =0,032 mol.
Quantité de matière théorique d'oxalate de diphényle : 0,0133 mol.
M(Oxalate de diphényle) =242 g / mol.
Masse théorique : 0,0133 x 242 = 3,2 g.
Rendement = masse réelle / masse théorique = 2,8 / 3,2 =0,88 ( 88 %).