Valorisation
des déchets d'un méthaniseur, Bac S Centres étrangers 2018
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
|
|
.
.
|
|
1. Maintien à température du digestat.
Une
partie du méthane produit est utilisé pour chauffer le méthaniseur. La
température doit être maintenue à une valeur proche de 38°C.
Le méthaniseur est assimilable à un cylindre en béton armé, d'épaisseur e1 = 30 cm, d'un diamètre D = 10,0 m et d'une hauteur h = 5,0 m. Il est isolé par l'extérieur avec du polystyrène d'épaisseur e2 = 15 cm. Un bardage en bois d'épaisseur e3
= 2,0 cm protège le dispositif des intempéries. La poche de biogaz au
sommet de l'ensemble est retenue par une membrane étanche.
Conductivité thermique en W m-1 K-1 : lbéton = 1,65 ; lpolystyrène = 0,038 ; l bois = 0,20.
1.1. Déterminer le mode de transfert thermique à travers les parois latérales du méthaniseur.
Transfert par conduction thermique.
1.2 Vérifier que la résistance thermique totale de la paroi latérale Rtotale est égale à 2,7 10-2 SI. Préciser son unité.
Les résistances thermiques des parois accolées s'additionnent.
Rtotale =( e1 / lbéton + e2 / lpolystyrène / e2 +e3 / l bois) / S.
S = p D h = 3,14 x10 x 5 = 157 m2.
Rtotale = (0,30 / 1,65 + 0,15 / 0,038 + 0,020 / 0,2) / 157 =0,02694 ~2,7 10-2 K W-1.
1.3. La température moyenne de l'air est10°C.
1.3.1. Représenter le flux thermique F à travers la paroi verticale du méthaniqeur par une flèche. Justifier.
Le flux thermique est dirigé du digestat ( corsps chaud 38°C) vers l'air extérieur ( corps froid 10°C).
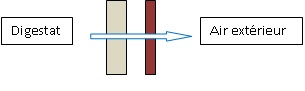
1.3.2. Calculer la valeur de ce flux.
F = (T2-T1) / Rtotale = (38-10) / (2,694 10-2) 1039 W~1,0 kW.
1.4. Un méthaniseur de cette taille peut produire 750 000 m3 de biogaz par an. L'énergie que peut produire 1 m3
de biogaz vaut 21 MJ. Les pertes thermiques totales sont évaluées à 1,6
kW en moyenne. Comparer la valeur de l'énergie stockée sous forme de
biogaz aux pertes thermiques de l'installation. Commenter.
Pertes thermiques par an : 1,6 x365 x24 x3600 ~5,0 107 kJ = 5,0 104 MJ.
Energie stockée : 750 000 x 21 ~1,6 107 MJ.
5,0 104 / 1,6 107 x100 ~0,3 %.
Les pertes ( donc l'énergie nécessaire à maintenir à 38°C le digestat ) représentent 0,3 % de l'énergie stockée.
|
|
...
|
|
|
|
|
2. Le digestat, un engrais vert.
Un laboratoire analyse un digestat afin de connaître sa teneur en azote N.
1 kg de digestat est chauffé et brassé. L'ammoniac issu du digestat est
recueilli puis dissous dans de l'eau acidifiée. Lorsque la totalité de
l'ammoniac s'est échappée du digestat, on recueille l'intégralité de la
solution S formée, de volume VS = 2,0 L. Le pH de cette solution est voisin de 5.
2.1 Identifier l'espèce azotée majoritaire dans la solution S.
pKa ( ion ammonium NH4+ / ammoniac NH3 )= 9,2.
A pH inférieur à pKa, la fome acide NH4+ prédomine.
2.2. On dose un volume V = 10,0 mL de solution S par une solution d'hydroxyde de sodium de concentration Cb = 0,10 mol/L. Le suivi pH méttrique donne la courbe suivante.
2.2.1 Ecrire l'équation de la réaction support du dosage.
NH4+ aq + HO- aq --> NH3aq + H2O(l).
On suppose que seule cette réaction se produit lors du dosage.
2.2.2. Le
laboratoire indique une teneur en azote égale à 2,6 g par kilogramme de
digestat. Cette teneur est-elle cohérente avec le suivi-pHmétrique ?
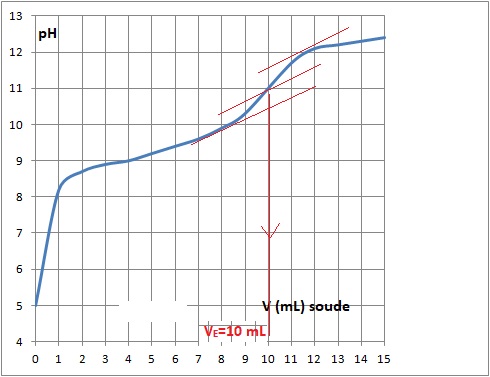
A l'équivalence : quantité de matière d'ion hydroxyde : 10 x 0,10 = 1,0 mmol.
Quantité de matière d'ion ammonium : 1,0 mmol dans 10 mL soit 200 mmol
= 0,20 mol dans 2,0 L de solution S, c'est à dire dans 1 kg de digestat.
Soit une masse d'azote de 0,20 x M(N) = 0,20 x14 =2,8 g.
Ecart relatif : (2,8-2,6) / 2,6 x100 ~7,8 %.
Cette valeur est en accord avec le suivi pH métrique.
|
|
2.3. L'agriculteur utilisait auparavant un engrais de synthèse, le nitrate d'ammonium NH4NO3.
Après avoir calculer la masse d'azote dans une mole de nitrate
d'ammonium, comparer les apports en azote du digestat et de cet engrais
de synthèse puis donner un avantage et un inconvénient de la
valorisation du digestat comme engrais.
M(NH4NO3) =2 x14 +3 x16 +4 =80 g /mol.
Masse d'azote correspondante : 28 g dans 80 g d'engrais.
Soit 28 / 80 x1000 = 350 g d'azote dans 1 kg de nitrate d'ammonium.
350 / 2,6 ~ 900 ;
1 kg de nitrate d'ammonium apporte 900 fois plus d'azote qu'un kilogramme de digestat.
L'ammoniac est plus facilement utilisable par les plantes ; le digestat
contient en plus de la matière ligneuse contribuant à la formation de
l'humus.
Coût du digestat : néant, alors que l'engrais coûte cher.
|
|