|
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts. |
||
| .
. |
||
|
||
|
|
Dans une rue plane et rectiligne, un motard M dťmarre quand le feu passe au vert avec une accťlťration de valeur a1 pendant la durťe S ; ensuite le pilote maintient sa vitesse constante de valeur v1. A l'instant du dťmarrage du cyclomoteur, une automobile A, situťe ŗ la distance D du feu, derriŤre M, roule ŗ vitesse constante , de valeur v2. On choisit comme origine des espaces, la position du feu tricolore, et comme origine des temps, l'instant oý l'auto pase devant le feu tricolore. Le sens positif de l'axe correspond au ens du mouvement.
a1 = 1 m/s≤ ; v2 = 10 m/s ; D= 10 m ; 80Ĺ= 8,9 ; S = 20 s. corrigť nature du mouvement du motard pendant la premiŤre phase de son dťplacement : mouvement rectiligne uniformťment accťlťrť. La vitesse v est une primitive de l'accťlťration : v est de la forme a1 t ; soit en tenant compte de l'origine des dates : v = a1( t+T) la position xM du motard est une primitive de la vitesse : xM est de la forme Ĺa1t2 ; xM = Ĺa1( t+T)2 et en combinant ces deux relations ( ťliminer le temps): v2 =2 a1xM . durťe T nťcessaire pour que A atteigne le feu : T= D/v2 = 10/10 = 1 s. ťquation horaire xM(t) du motard pout t<= S-T en fonction de a1, D et v2 : xM(t) = Ĺa1(T+t)2 = Ĺa1(D/v2+t)2 ; xM(t) = 0,5 (1+t)2 . ťquation horaire xA(t) de l'auto : xA(t) = v2 t = 10 t. date t1 ŗ laquelle l'auto rattrape la moto : xA(t1)=xM(t1) 0,5(1+t1)2= 10 t1 ; t12 -18t1+1=0 deux solutions : t= 0,1 s et t= 17,9 s. ŗ la date t= 0,1 s, la voiture dťpasse la moto ; ŗ la date t = 17,9 s, la moto dťpasse ŗ nouveau la voiture. Pour t>=S-T soit t> 19 s, la moto est en tÍte. position de la moto pour t= S-T soit t = 19 s : xM(19) = 0,5*20≤ = 200 m. ťquation horaire du motard pour t>=19 s : mouvement rectiligne uniforme ŗ la vitesse v = a1S = 20 m/s.
|
|
|
|
||
|
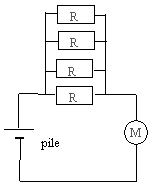
On dispose du matťriel suivant : une pile "9 V", cinq conducteurs ohmiques de rťsistances R= 20 W, deux multimŤtres, des fils, un jouet ( petite grue dotť d'un moteur ťlectrique), une notice du moteur de la grue sur laquelle on peut lire " puissance ťlectrique maximale tolťrťe = Pmax = 3 W". Tension aux bornes du moteur ťlectrique U= E'+ r' I avec E' : force ťlectromotrice du motuer et r': rťsistance ťlectrique du moteur Etude de la pile : on rťalise un montage qui permet de tracer la caractŤristique intensitť-tension de la pile, c'est ŗ dire la courbe reprťsentant l'ťvolution de la tension UPN aux bornes de la pile en fonction de l'intensitť I qu'elle dťbite. 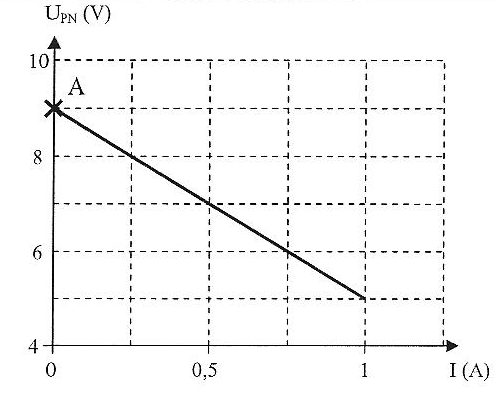
Etude du moteur de la grue : on dťcide de faire fonctionner le moteur gr‚ce ŗ la pile de 9 V.
Utilisation de la grue : une charge de masse m= 1 kg est posťe au sol, ŗ cŰtť de la grue ; le fil indťformable est tendu. 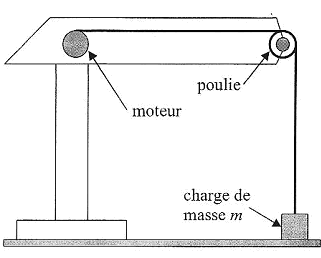 On fait tourner le moteur ťlectrique pendant t= 5,0 s, ce qui a pour effet d'enrouler le fil sur l'arbre du moteur et ainsi de lever la charge d'une hauteur totale h= 75 cm. On considŤre que le mouvement de la charge est rectiligne et uniforme pendant la montťe. L'intensitť du courant dans le circuit vaut I= 0,5 A. g = 10 m/s≤.
valeurs de la fem E et de la rťsistance interne r de la pile : E= 9 V ( ordonnťe du point A) pente de la droite :-4/1 = -4 V A-1 ; d'oý r = 4 W. On relie brievement les deux bornes de la pile par un fil de jonction : UPN=0 soit Imax = E/r = 9/4 = 2,25 A. on monte en sťrie la pile et deux conducteurs ohmiques
de rťsistance R : E-r I
= 2RI soit I = E/(2R+r) = 9/44 = 0,20
A.
Puissance absorbťe par le moteur : P= UPN I= 6*0,75 = 4,5 W, valeur bien supťrieure ŗ 3W, Pmaxi que peut supporter le moteur : celui-ci va Ítre grillť. on rťaliser un dipŰle ohmique de rťsistance R' = 5 W en branchant 4 rťsistors de rťsistance R= 20 W en dťrivation.
tension aux bornes de la pile durant la montťe de la charge : UPN= E-rI = 9-4*0,5 = 7 V. ťnergie ťlectrique fournie par la pile en 5 s : UPN I t = 7*0,5*5 =17,5 J diminution d'ťnergie chimique contenue dans la pile : E I t = 9*0,5*5 = 22,5 J. expression de la puissance mťcanique Pm que dťveloppe le moteur durant la montťe : Mouvement rectiligne uniforme : les deux forces appliquťe ŗ la charge m ont la mÍme valeur et sont opposťes ( d'aprŤs le principe d'inertie ) Donc, la valeur absolue du travail du poids est ťgal au travail de la tension du fil : W = mgh Or la puissance (W) est ťgale au travail (J) divisť par la durťe (s) ; d'oý Pm = mgh/5 = 1*10*0,75 / 5 =1,5 W. expression de la fcem E' du moteur en fonction de Pm : E' = Pm / I = 1,5 / 0,5 = 3 V.
|
||
|
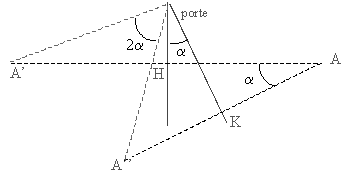
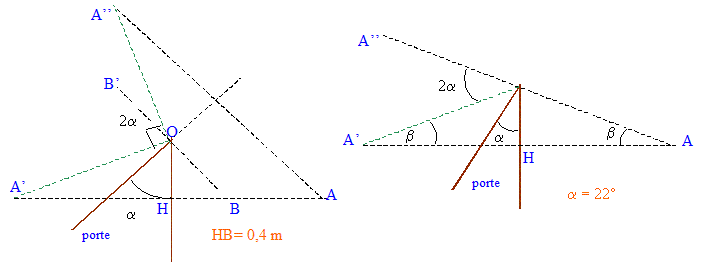
Une porte de 80 cm de large est recouverte d'un miroir. Un observateur situť ŗ 1,00 m en face de cette porte fermťe observe son image. Une autre personne ouvre la porte : le centre de la porte s'ťloigne alors de l'observateur immobile qui perd rapidement de vue son image. En assimilant l'observateur ŗ un point A situť sur la normale au plan de la porte fermťe passant par son centre :
corrigť A' image de A quand la porte est fermťe ( A et A' sont symťtriques par rapport au plan de la porte) A'" image de A quand la porte est fermťe ( A et A'' sont symťtriques par rapport au plan de la porte)
Dťs que l'image A" sort du champ visuel de l'observateur, ce dernier ne se voit plus dans le miroir.
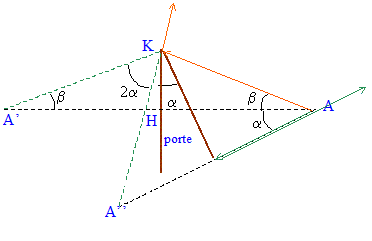
tan b = 0,4/1 = 0,4 soit b =21,8 į ; AK = (1≤ + 0,4≤)Ĺ=1,077 m sin ( a+b) = 0,8 / 1,077 = 0,743 soit a+b = 48 į ; d'oý a = 48-21,8 = 26,2į.
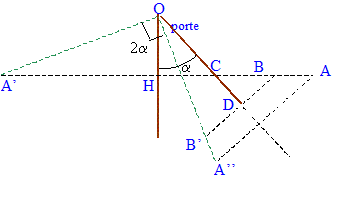
L'observateur doit venir en B afin de voir son image B'. Dans les triangles OHC et DBC : OC = 0,4*2Ĺ =0,566 m ; CD= DB = 0,8-0,566 = 0,234 m CB = 0,234*2Ĺ = 0,33 m soit HB= 0,4+0,33 = 0,73 m ouverture en sens contraire :
|
||
|
Le carbonate de magnťsium est un composť ionique de formule MgCO3 peu soluble dans l'eau. On essaie de dissoudre un peu de ce solide dans l'eau.
corrigť MgCO3 (s) = Mg2+(aq) + CO32-(aq) constante K associťe ŗ cette ťquation : K =[Mg2+][CO32-] = s≤ d'oý s = (10-5)Ĺ =10-2,5 = 0,3 10-2 = 3 10-3 mol/L. quotient de rťaction initial correspondant ŗ l'ťquation ťcrite en 1 : Q r i = [Mg2+]i [CO32-]i [CO32-]i = s = 3 10-3 mol/L ; n( Mg2+) = 3 10-3*0,1 + 1,0 10-3 =1,3 10-3 mol ; [Mg2+]i =1,3 10-3 / 0,1 = 1,3 10-2 mol/L Q r i = 3 10-3*
1,3 10-2 = 3,9 10-5
; Q r i >K, donc ťvolution dans le sens
indirect, de la droite vers la gauche.
n (Mg2+) total = m/84 +10-3 mol ; [Mg2+] = m/84 +10-3 mol /L ; [CO32-] = m/84 mol/L ŗ l'ťquilibre : K= (m/84 +10-3 ) * m/84 ; on pose x = m/84 d'oý x≤ + 10-3 x-10-5 = 0 ; retenir la solution positive x = 2,7 10-3 mol. |
||
|
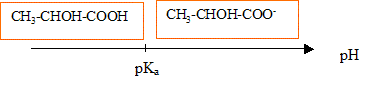
L'acide lactique a pour formule CH3-CHOH-COOH. On prťpare 50,0 mL d'une solution aqueuse S d'acide lactique de concentration molaire cA= 2,00 10-2 mol/L. Le pH de cette solution vaut pH= 2,8.
zone de virage phťnolphtalťine : incolore [8,2- 9,8] rose corrigť les groupes fonctionnels prťsents dans la molťcule ; -COOH acide carboxylique ; C-OH : alcool secondaire. deux couples acide /base qui interviennent quand on dissout de l'acide lactique dans l'eau : CH3-CHOH-COOH / CH3-CHOH-COO- : CH3-CHOH-COOH = CH3-CHOH-COO- + H+. H3O+/H2O : H3O+= H2O + H+. ťquation de la rťaction de l'acide lactique avec l'eau : CH3-CHOH-COOH + H2O = CH3-CHOH-COO- +H3O+. taux d'avancement final de la transformation : t = xfin / xmax. xmax = Ca*0,05 = 2 10-2*0,05 mol ; xfin = 10-pH*0,05 = 10-2,8*0,05 mol t = 10-2,8 / 2 10-2 = 0,5*10-0,8 = 0,5*0,16 = 0,08. La transformation est partielle car t <<1. domaines de prťdominance de l'acide lactique et de son espŤce conjuguťe
ŗ pH=2,8 la forme acide prťdomine. A partir de la question 3: 8% de forme ion lactate et 92% de la forme acide lactique.
volume de solution d'hydroxyde de potassium ŗ ajouter pour observer le changement de couleur : ŗ l'ťquivalence les quantitťs de matiŤre des rťactifs mis en prťsence sont en proportions stoechiomŤtriques : CaVa = CbVb soit Vb = CaVa / Cb=0,02*20 / 0,05 = 8 mL. changement de couleur observť : dans l'erlenmeyer, avant l'ťquivalence, l'acide lactique est en excŤs ( solution incolore) ; aprŤs l'ťquivalence, les ions HO- sont en excŤs ( couleur rose).
|
||
|
|