|
Oxydo-rťduction
: ťtude cinťtique de la dismutation de l'eau
oxygťnťe bac
S 2007 La Rťunion |
|||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||
|
L'eau oxygťnťe commerciale est une solution aqueuse de peroxyde d'hydrogŤne utilisťe comme dťsinfectant pour les plaies, pour l'entretien des lentilles de contact ou comme agent de blanchiment. Le peroxyde d'hydrogŤne H2O2 intervient dans deux couple oxydant-rťducteur : H2O2(aq) / H2O et O2 (g) /H2O2(aq) Le peroxyde d'hydrogŤne est capable dans certaines conditions de rťagir sur lui mÍme c'est ŗ dire de se dismuter selon l'ťquation : 2H2O2(aq) =2H2O + O2(g) (1) Cette rťaction est lente ŗ tempťrature ordinaire mais sa vitesse peut Ítre augmentťe en prťsence d'un catalyseur. Donnťe : volume molaire des gaz Vm=25 L/mol. Etude de la rťaction de dismutation : Ecrire les deux demi-ťquations d'oxydo-rťduction des couples auxquels le peroxyde d'hydrogŤne appartient. Etablir un tableau d'ťvolution du systŤme. Dťtermination de la concentration initiale de la solution de peroxyde d'hydrogŤne : L'eau oxygťnťe du commerce se prťsente en flacon opaque afin d'ťviter que la lumiŤre favorise la transformation chimique prťcťdente. Le flacon utilisť dans cette ťtude porte la mention suivante : eau oxygťnťe ŗ 10 volumes. Cette indication est appelťe le titre de l'eau oxygťnťe. Par dťfinition le titre est le volume de dioxygŤne ( exprimť en litre) libťrť par un litre de solution aqueuse de peroxyde d'hydrogŤne suivant la rťaction (1) dans les conditions normales de tempťrature et de pression. On considŤrera en premiŤre approximation que les conditions de l'expťrience sont assimilables aux conditions normales. Avant de rťaliser le suivi cinťtique de la rťaction de dismutation, on dťsire vťrifier l'indication donnťe sur le flacon concernant le titre de l'eau oxygťnťe de la solution commerciale utilisťe.
Etude de la rťaction de dismutation : L'oxydant H2O2(aq) se rťduit en gagnant des ťlectrons : H2O2(aq) + 2H++2e- = 2 H2O Le rťducteur H2O2(aq) s'oxyde en cťdant des ťlectrons : H2O2(aq) = O2 (g) + 2H++2e-. Bilan : 2H2O2(aq) = 2 H2O + O2 (g) Tableau d'ťvolution du systŤme :
Dťtermination de la concentration initiale de la solution de peroxyde d'hydrogŤne : D'aprŤs la dťfinition du titre de l'eau oxygťnťe le volume de dioxygŤne V(O2) libťrť par un volume V= 1,00 L de la solution commerciale au cours de la rťaction de dismutation du peroxyde d'hydrogŤne est ťgal ŗ l'indication portťe sur le flacon . V(O2) = 10
L. n(O2) = V/Vm = 10 / 25 ;
xf = n(O2) =
0,40 mol. n0(H2O2)-2xf =0 soit n0(H2O2)=2xf = 0,80 mol dans 1 L de solution [H2O2]th = 0,80 mol/L. Dťtermination de la
valeur rťelle de la concentration en peroxyde
d'hydrogŤne : L'ion permanganate est la seule espŤce colorťe ; il joue un double rŰle: - celui de rťactif ( solution titrante) se trouvant dans la burette - celui d'indicateur de fin de rťaction : avant l'ťquivalence, dans le becher, l'ion MnO4-(aq) est en dťfaut, la solution est incolore. AprŤs l'ťquivalence, dans le becher, l'ion MnO4-(aq) est en excŤs , la solution est violette. A l'ťquivalence on observe un changement de teinte, passage d'une solution incolore ŗ une solution violette. Relation entre la quantitť initiale de peroxyde d'hydrogŤne se trouvant dans le becher n0(H2O2) et la quantitť d'ions permanganate introduits dans le becher ŗ l'ťquivalence neq(MnO4-) :
neq(MnO4-) -2xťqui=0 donne : xťqui= Ĺneq(MnO4-) n0(H2O2)-5xťqui=0 donne n0(H2O2)=5xťqui=2,5 neq(MnO4-) n0(H2O2)=2,5 neq(MnO4-). neq(MnO4-) = c1 Veq=2,0 10-1 * 14,6 10-3 = 2,92 10-3 mol. n0(H2O2)= 2,5*2,92
10-3 = 7,3 10-3 mol L'ťcart avec la valeur thťorique est proche de 10 % : l'eau oxygťnťe a ťtť prťparťe depuis un certain temps et la dismutation du peroxyde d'hydrogŤne est dťja bien avancťe.
La dismutation est une rťaction lente mais qui peut Ítre accťlťrťe en utilisant par exemple des ions fer (III) Fe3+(aq) prťsents dans une solution de chlorure de fer III, un fil de platine ou de la catalase, enzyme se trouvant dans le sang.
|
|||||||||||||||||||||||||||||||||||||||||||||||||
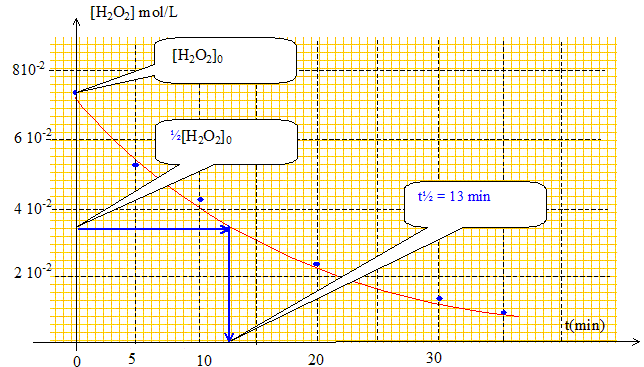
Un catalyseur est une espŤce qui accťlťre une transformation chimique lente, mais spontanťe ; il n'apparaÓt pas dans le bilan : il est rťgťnťrť en fin de rťaction. La catalyse rťalisťe par un fil de platine est hťtťrogŤne : milieu rťactionnel liquide et catalyseur solide. Graphe traduisant l'ťvolution de la concentration en peroxyde d'hydrogŤne en fonction du temps :
Avancement de la transformation x(t) en fonction de nt(H2O2) quantitť de peroxyde d'hydrogŤne prťsent ŗ l'instant t et de n0(H2O2) quantitť initiale de peroxyde d'hydrogŤne :
La vitesse volumique v de la transformation chimique est dťfinie comme ťtant le rapport de la dťrivťe de l'avancement x(t) en fonction du temps par le volume V du systŤme : v = 1/V d x(t) / dt. n0(H2O2) ťtant une constante, sa dťrivťe est nulle d'oý : d x(t) / dt =-Ĺ d nt(H2O2) /dt v = -Ĺ 1/V d nt(H2O2) /dt De plus [H2O2] =
nt(H2O2)
/ V d'oý : v = -Ĺ
d[H2O2]/dt. -d[H2O2]/dt est le coefficient directeur de la tangente au point considťrť, ŗ la courbe ci-dessus. Or au cours du temps ces tangentes sont de moins en moins inclinťes par rapport ŗ la verticale : le coefficient directeur diminue, donc la valeur de la vitesse diminue. De plus la concentration en peroxyde d'hydrogŤne est un facteur cinťtique : au cours du temps [H2O2] diminue et en consťquence la vitesse de la transformation diminue. Temps de demi-rťaction tĹ : Durťe au bout de laquelle l'avancement est ťgal ŗ la moitiť de l'avancement final. La transformation est totale donc xfin = xmax. n0(H2O2)-2xmax=0 soit xmax = Ĺ n0(H2O2) n0(H2O2)/ V = [H2O2]0 ; ntĹ(H2O2)/ V = [H2O2]tĹ ; ntĹ(H2O2) / V =Ĺ n0(H2O2) / V = Ĺ[H2O2]0 A t= tĹ alors [H2O2]tĹ =Ĺ[H2O2]0. La tempťrature est un facteur cinťtique :
si la tempťrature augmente, la vitesse de la
rťaction augmente et en consťquence le temps
de demi rťaction sera infťrieur ŗ la
valeur prťcťdente.
|
|||||||||||||||||||||||||||||||||||||||||||||||||
|
|