|
acide, base, pH En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées ŕ vos centres d’intéręts. |
|||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||
|
Domaines d'acidité et de basicité en solution aqueuse. Le pH permet de déterminer si une solution est acide, neutre ou basique. Les valeurs usuelles du pH sont comprises entre 0 et 14. A 25 °C, une solution est acide si son pH est inférieur ŕ 7, neutre si son pH vaut 7, basiquesi son pH est supérieur ŕ 7. Une solution a un pH égal ŕ 10. Est-elle acide, neutre ou basique. Le pH étant supérieur ŕ 7, la solution est basique. Le jus de citron est acide. Dans quel domaine se situe la mesure de son pH ? Une solution acide a un pH inférieur ŕ 7. Le pH du jus de citron est compris entre [0 ; 6,9 ], sans doute vers pH=3 ou pH = 4. Une solution aqueuse neutre contient autant d’ions hydrogčne H+ que d’ions hydroxyde HO-. Dans une solution acide, il y a plus d’ions hydrogčne H+ que d’ions hydroxyde HO-. Dans une solution basique, il y a plus d’ions hydroxyde HO- que d’ions hydrogčne H+. Les produits acides ou basiques concentrés présentent des dangers. Couper un petit morceau de papier pH et le
mettre sur un support propre. Déposer une goutte de la solution
étudiée sur le papier pH. Comparer la couleur obtenue ŕ
l'échelle de teintes.
Quelle est le pH approximatif de la solution ? Le pH de la solution est compris entre pH=3 et pH= 5. Cette expérience nous renseigne t-elle sur la couleur de la solution ? Cette expérience fournit une indication sur la nature du milieu, acide, neutre ou basique. Elle n'apporte pas de renseignement sur la couleur de la solution. De plus il vaut mieux utiliser l'échelle de teintes du papier pH avec une solution incolore, sinon la teinte obtenue serait faussée par la couleur de la solution. L'expérience nous permet-elle de connaître la nature de la solution ? On peut bien entendu éliminer un certain nombre de solutions telles que : eau de source ( pH proche de 7), eau de lessive ( pH voisin de 8 ou 9). On peut identifier la solution ŕ une boisson acide, ŕ un jus de citron. Mais l'expérience ne permet pas d'identifier les espčces présentes en solution.
Compléter le tableau suivant : ( présence d'ion H+ en grande
quantité) ( présence d'ion HO+ en grande
quantité)
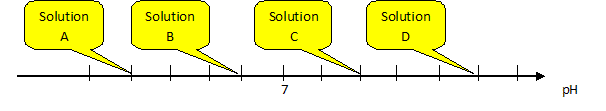
La solution A possčdant le plus petit pH ( pH = 3) est la plus acide. La solution D possčdant le plus grand pH ( pH = 12) est la plus basique. Quelle est la nature de chaque solution ? Choisir parmi ( jus de citron dilué, acide chlorhydrique, solution de soude concentrée, eau de Javel. a : acide chlorhydrique ; B jus de citron dilué ; C : eau de javel ; D : solution de soude concentrée.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||
|
|