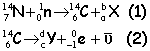voir le match : ce qu'il faut retenir
mots croisés
|
|
|
|
électronvolt : 1 eV énergie acquise par un électron accéléré sous une tension de 1 V 1 eV=1,6 10-19 J E=mc² la masse est une forme de l'énergie. j'exprime 1 u en MeV c-2 1,66 10 -27 * (3 108 )² =1,4 10-10 J 1,4 10-10*1,6 10-19 =931,5 MeV (M=106) 1 u=931,5 MeVc-2 |
loi de décroissance radioactive
A :
activité en Becquerel Bq
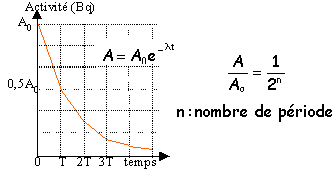
nombre moyen de désintégrations par seconde.
T : période radioactive ou demi vie
durée au bout de laquelle l'activité est égale à la moitié de sa valeur initiale.

- Calculer le rayon d'un noyau de l'élément cuivre (A=63 )
- Calculer la masse volumique de ce noyau dont la masse est voisine de 63 u
corrigé
rayon du noyau R= 1,2 *63 exp (1/3) = 4,8 fm = 0,48 10-14 m
masse du noyau : 63*1,66 10-27 = 1,05 10-25 kg
volume du noyau (sphère): 4/3*3,14 (0,48 10-14 ) 3= 4,6 10-43 m3.
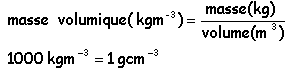
1,05 10-25 / 4,6 10-43 = 2,28 1017 kgm-3.
trés grande comparée à celle du métal cuivre 8900 kgm-3.
|
|
|
|
|
|
L'énergie de liaison par nucléon est voisine de 8 MeV pour la majorité des nucléides.
- Quelle est l'énergie de liaison par nucléon d'un noyau d'uranium 235.
corrigé
masse des constituants du noyau , séparés au repos
92 protons : 92*1,007 276 = 92,669 392 u
235-92= 143 neutrons
143* 1,008 665 = 144,239 095 u
92,669 392 + 144,239 095 = 236,908 487 u
défaut de masse :
235 :234,994 - 236,908 487 = - 1,915 u
1,915 / 235 = 8,14 10-3 u par nucléon
énergie de liaison par nucléon
8,14 10-3 *931,5 = 7,6 MeV par nucléon
réaction de fission
![]()
|
collision entre un neutron lent et un noyau d'uranium
U: 235,043 915 u; Ba : 141,916 350 ; Kr : 89,819 720 u ; neutron : 1,008 665 u |
|
|
corrigé conservation de la charge : 92 + 0 = 36 + Z + y*0 d'où Z= 56 conservation du nombre de nucléons : 235 + 1 = 90 + 142 + y d'où y= 4 masse des réactifs : 235,043 915 + 1,008 665 = 236, 052 58 u masse des produits : 89,819 720 + 141,916 350 + 4,034 660 = 235,870 730 u défaut de masse : 235,870 730 - 236,052 58 = -0,28 185 u énergie libérée par noyau d'uranium 0,28 185 *931,5 = 262 MeV 262 106 * 1,6 10-19 = 4,19 10-11 J énergie libérée par mol d'uranium (235 g) 4,19 10-11 * 6,02 1023= 2,5 10 13 J ou 1,07 1014 J par kg puissance du réacteur = 10 8 watt ou 108 joules par seconde 1 kg d'uranium libère 1,07 1014 J 1,07 1014 / 108 = 1,07 106 s ou 12,2 jours. |
![]()
masse H: 1,007 3 u ; He : 4,0015 u ; positon ou bien électron 0,55 10-3 u |
|
|
corrigé conservation de la charge : 4=2+2x d'où x=1 il s'agit d'un positon (électron positif)
masse initiale : 4*1,007 3= 4,029 2 u masse finale des produits : 4,001 5 +2*0,55 10-3 = 4,002 65 u perte de masse : 4,002 65-4,029 2 = -0,026 6 u ou -0,026 6*1,66 10-27 = -4,41 10-29 kg énergie libérée : 0,026 6* 931,5 = 24,8 MeV 24,8 *1,6 10-19 = 4 10-12 J par réaction La puissance est l'énergie libérée chaque seconde soit : 3,9 1026 J pour une perte de 4,41 10-29 kg l'énergie libérée est 4 10-12 J diminution de masse du soleil à chaque seconde: 3,9 1026 / 4 10-12 *4,41 10-29 =4,3 106 tonnes expression de l'âge du soleil en seconde : 4,6 109*365*24*3600= 1,45 1017 s diminution de masse du soleil : 1,45 1017 * 4,3 106 = 6,2 1023 tonnes soit en pourcentage de la masse du soleil : 6,2 1026 / 2 1030 *100 = 0,03 % |
1. Une certaine substance radioactive dont la demi-vie est de 10 s émet 2.107 particules alpha par seconde.
- Calculer la constante de désintégration de cet isotope.
- Calculer l'activité de cette substance Bq .
- Combien y a-t-il de noyaux radioactifs dans cette substance ?
- Combien en restera-t-il après 30 secondes ?
2 . On mesure en laboratoire l'activité spécifique de 235U. On trouve que 1 mg d'un échantillon d'Uranium 238 U émet 740 particules alpha/minute. Calculer la constante de désintégration de l'238U et sa période.
corrigé
demi vie ou période = 10 s
constante radioactive fois période = ln 2 =0 ,693
constante radioactive = 0,693 / 10 = 0,069 s-1.
activité = nombre de désintégrations par seconde = 2 107 Bq
nombre de noyaux radioactifs à la date t =0 : (instant de la mesure de l'activité)
A = l N0 donne N0 = 2 107 /0,069=2,9 108 noyaux à t=0 .
30 seconde c'est trois périodes
au bout d'une période : il reste ½ 2,9 108 noyaux ( la moitié a disparu)
au bout de 2 périodes, 2,9 108 / 4 noyaux.
pour 3
périodes , 2,9 108 / 8 =
3,6 107 noyaux.
masse (g) / masse molaire (g/mol) quantité de
matière (mol)
0,001 / masse molaire = 0,001 / 238 = 4,2 10-6 mol
une mole d'atomes contient 6,02 1023 atomes
4,2 10-6 *6 ,02 1023 = 2,52 1018 noyaux d'uranium dans 1 mg
au bout d'une période la moitié est désintégré soit 1,26 1018 noyaux
740 désintégrations en une minute, d'où la période : 1,7 1015 minutes
ou 3,3 109 années
constante radioactive fois période = 0,693 = ln 2
constante
radioactive = 0,693 / 3,3 109 = 2,1
10-10 années-1.
exercice 7 :
|
|
|
|
|
|
|
|
|
|
|
|
- Indiquer la composition de ces deux noyaux et écrire les deux équations des désintégrations radioactives.
- La période de désintégration ou
demi-vie du plomb 214 est T1 = 27 min.
- En déduire la valeur de la constante radioactive l1 en s-1.
- Calculer l'activité d'un échantillon contenant 1 ng de plomb 214 sachant qu'il contient 2,8 1012 noyaux de plomb 214. - On considère maintenant un échantillon contenant à t=0 autant de noayaux de plomb 210 que de noyaux de plomb 214. La période de désintégration ou demi-vie du plomb 210 est T2 = 22 ans. On note A1 l'activité du plomb 214 et A2 celle du plomb 210. t = A2/A1.Calculer t à t=0 et à t = 27 min.
plomb 210 : 82 protons et 210-82 =128 neutrons
plomb 214 : 82 protons et 214-82 =132 neutrons
21082Pb--> 21083Bi + -10e
21482Pb--> 21483Bi + -10e
T1l1 = ln2 soit l1 = ln2 / (27*60) = 4,3 10-4 s-1.
A = Nl1 = 2,8 1012 * 4,3 10-4 = 1,2 109 Bq.
t = A2/A1= N2l2 / (N1l1 )=N2 T1 / (N1T2 )
à t = 0, N1 = N2 d'où t = T1 / T2 = 27 / (22*365*24*60) = 2,33 10-6.
à t = 27 min, N1 est divisée par deux tandis que N2 reste pratiquement inchangée (22 min <<22 ans)
d'où t
double soit = 4,66 10-6.
DONNÉES :1 u (unité de masse atomique) = 1,6606 10-27 kg ; c = 3 108 m.s-1 ;NA = 6,022 1023 mol-1 ; e =1,6 10-19 C ;
Masses de quelques particules :mproton = 1,6726 10-27 kg ; mneutron = 1,6749 10-27 kg
Masses atomiques de quelques isotopes :23592U =235,044 u ; 14658Ce =145,910 u ;8534Se = 84,922 u
- Les réacteurs
nucléaires. La France
compte aujourd'hui 58 réacteurs nucléaires
à eau sous pression (REP). La production
d'énergie dans ces réacteurs repose sur la
fission de l'uranium 235. En effet, lorsqu'un neutron
heurte un noyau d'uranium 23592U,
une des fissions possibles conduit à la formation
d'un noyau de cérium 14658Ce
et d'un noyau de sélénium
8534Se, ainsi qu'à un nombre
a de neutrons. Écrire l'équation
complète de cette réaction nucléaire
; en déduire la valeur de a. Justifier en
exprimant les lois appliquées.
- Calculer la variation de masse Dm qui accompagne la fission d'un noyau d'uranium 235.
- Calculer, en joule et en MeV, l'énergie E libérée par cette réaction. - Les centrales nucléaires françaises utilisant de l'uranium 235 fournissent au maximum une puissance électrique P = 1455 MW. La combustion d'un kilogramme de pétrole libère une énergie E = 45 106 J sous forme de chaleur. Le rendement de la transformation d'énergie thermique en énergie électrique est de 34,2 %. En déduire la masse de pétrole qui serait nécessaire pour produire pendant un an la même énergie électrique que les centrales nucléaires françaises.
- Étude des déchets
et radioprotection La
fission de l'uranium 235 produit, entre autres
nucléides, le césium 137, émetteur
radioactif g.
Un employé de la centrale reste accidentellement
durant une heure à proximité de la source
de 1,0 g de césium 137. Durant cette exposition,
il absorbe, uniformément sur l'ensemble du corps,
5 % des rayons g
d'énergie 0,66 MeV émis par cette source.
On suppose que l'activité de cette source est
égale à 3,0 1012 Bq. Sachant que
l'employé a une masse de 70 kg, calculer la dose
absorbée en gray (ou J.kg-1).
- La notion de dose n'est pas suffisante pour expliquer les relations " doses-effets ". C'est pourquoi on lui assortit un paramètre " qualité " du rayonnement traduisant la nature du rayonnement incident. Ainsi le produit de ce coefficient appelé EBR par la dose absorbée traduit une " dose équivalente " exprimée en sievert (Sv) ; la dose maximale annuelle autorisée est de 50 mSv. Calculer la dose absorbée reçue par l'employé de la centrale victime de l'accident sachant que l'EBR vaut dans ces conditions 0,06. Commenter ce resultat.
23592U + 01n = 14658Ce + 8534Se + a 01n
conservation de la charge : 92 +0 = 58+34 +a*0
conservation du nombre de nucléons : 235 +1 = 146 +85 + a soit a = 5
Dm = |masse produits - masse des réactifs|
D m = |145.910+84.922+4*1.0086-235.044|=0,1776 u
multiplier par 1,66 10-27 = 2,94 10-28 kg
E= D m c² = 2.94 10-28*9 1016 = 2,653 10-11 J
diviser par 1,6 10-13 :
165,8
MeV.
puissance (watt) * durée (seconde) = énergie
(J)
1,455 109 3600*24*365 = 4,6 1016 J
pour un kg de pétrole on produit : 4,5 10 7*0,342 = 1,54 107 J électrique
masse de pétrole : 4,6
1016 / 1,54 10 7 =
3 10 9
kg.
à chaque seconde 3 1012 noyaux de
césium se désintègrent libérant
une énergie de :
3 1012*0,66 = 1,98 1012 MeV
soit 1,98 1012*1,6 10-13 = 0,32 J
en une heure : 0,32*3600 = 1140 J
énergie reçue : 1140 *0,05 = 57 J
soit par kg : 57/70= 0,81 J/kg
dose équivalente: 0,81 *0,06 = 4,9 10-2 Sv = 49 mSv
à la limite de la dose annuelle autorisée.